REVISÃO DE LITERATURA
Modalidades Fisioterapêuticas no Manejo da Dor Neuropática Induzida pelo Tratamento do Câncer de Mama: Revisão da Literatura
Physiotherapeutic Modalities in the Management of Neuropathic Pain Induced by Breast Cancer Treatment: Literature Review
Modalidades Fisioterapéuticas en el Manejo Del Dolor Neuropático Inducido por el Tratamiento del Cáncer de Mama: Revisión de la Literatura
https://doi.org/10.32635/2176-9745.RBC.2024v70n1.4392
Julia Formentini Viesser1; Caroline Helena Lazzarotto de Lima2; Mariana Zancan3
1-3Universidade Regional Integrada do Alto Uruguai e das Missões. Campus Frederico Westphalen. Frederico Westphalen (RS) Brasil. E-mails: viesserjulia@gmail.com; carollima@uri.edu.br; marianazancan@gmail.com. Orcid iD: https://orcid.org/0009-0009-1854-2012; Orcid iD: https://orcid.org/0009-0002-1574-5681; Orcid iD: https://orcid.org/0000-0002-7082-2267
Endereço para correspondência: Julia Formentini Viesser. Avenida São Paulo, 1054, apto. 102 – Itapagé. Frederico Westphalen (RS) Brasil. CEP 98400-000. E-mail: viesserjulia@gmail.com
RESUMO
Introdução: A sobrevida de mulheres após o tratamento do câncer de mama tem aumentado em virtude de avanços na detecção precoce e terapias disponíveis. Porém, as sobreviventes comumente enfrentam efeitos adversos após o tratamento que representam grande carga física e psicológica. Além da fadiga, a dor é o sintoma persistente mais frequente após o tratamento. Objetivo: Sistematizar os resultados de ensaios clínicos randomizados sobre a intervenção fisioterapêutica na dor neuropática periférica induzida pelos tratamentos para o câncer de mama. Método: Busca realizada nas bases de dados MEDLINE via portal PubMed e Cochrane. Foram selecionados ensaios clínicos randomizados publicados a partir de 2017, em língua inglesa, que abordassem as modalidades fisioterapêuticas como intervenção, a dor neuropática periférica induzida por tratamentos oncológicos como desfecho, e mulheres sobreviventes ao câncer de mama como população de interesse. A qualidade metodológica dos estudos foi avaliada pela ferramenta Cochrane para o risco de viés. Resultados: Quatro estudos foram revisados na íntegra. Majoritariamente, os efeitos adversos do tratamento oncológico se devem a regimes quimioterápicos à base de taxanos. Os desfechos avaliados incluem, além da dor, demais sinais neuropáticos e influência nas atividades de vida diária. Os estudos variaram quanto à intervenção e fase de tratamento. Apenas um dos estudos demonstrou resultado significativamente positivo a favor do grupo intervenção. Conclusão: Estudos clínicos randomizados disponibilizam evidências escassas quanto aos efeitos positivos da intervenção fisioterapêutica na dor neuropática periférica induzida pelos tratamentos para o câncer de mama.
Palavras-chave: Manejo da Dor/métodos; Polineuropatia; Neoplasias da Mama; Antineoplásicos/farmacologia; Modalidades de Fisioterapia.
ABSTRACT
Introduction: Women's survival after breast cancer treatment has increased due to advances in early detection and available therapies. However, great physical and psychological burden are the result of adverse effects that survivors commonly face. In addition to fatigue, pain is the most common persistent symptom after cancer treatment. Objective: Systematize the results of randomized clinical trials on physiotherapeutic intervention in peripheral neuropathic pain induced by breast cancer treatments . Method: The search was carried out on the MEDLINE databases via PubMed and Cochrane portals. Randomized clinical trials published since 2017 in English, that addressed physiotherapeutic modalities as intervention, peripheral neuropathic pain induced by oncological treatments as outcome were selected, and the population of interest were women surviving breast cancer. The Cochrane-risk-of-bias tool was applied to evaluate the methodological quality of the studies. Results: Four studies were fully reviewed. Most of the adverse effects of cancer treatment are due to taxane-based chemotherapy regimens. The outcomes assessed include, in addition to pain, other neuropathic signs and influence on activities of daily living. The studies varied in terms of intervention and treatment phase. Only one of the studies demonstrated a significantly positive result in favor of the intervention group. Conclusion: Randomized clinical studies provide scant evidence regarding the positive effects of physiotherapeutic intervention on peripheral neuropathic pain induced by breast cancer treatments.
Key words: Pain Management/methods; Polyneuropathy; Breast Neoplasms; Antineoplastics/pharmacology; Physical Therapy Modalities.
RESUMEN
Introducción: La supervivencia de las mujeres después del tratamiento del cáncer de mama ha aumentado debido a los avances en la detección temprana y las terapias disponibles. Sin embargo, los supervivientes suelen enfrentarse a efectos adversos después del tratamiento que representan una gran carga física y psicológica. Además de la fatiga, el dolor es el síntoma persistente más común después del tratamiento del cáncer. Objetivo: Sistematizar los resultados de ensayos clínicos aleatorizados sobre intervención fisioterapéutica en el dolor neuropático periférico inducido por tratamientos para el cáncer de mama. Método: La búsqueda se realizó en las bases de datos MEDLINE a través de los portales PubMed y Cochrane. Se seleccionaron ensayos clínicos aleatorizados publicados desde 2017, en inglés, que abordaron modalidades fisioterapéuticas como intervención, dolor neuropático periférico inducido por tratamientos oncológicos como resultado y mujeres sobrevivientes de cáncer de mama como población de interés. La calidad metodológica de los estudios se evaluó mediante la herramienta Cochrane de Riesgo de Sesgo. Resultados: Se revisaron en su totalidad cuatro estudios. La mayoría de los efectos adversos del tratamiento del cáncer se deben a los regímenes de quimioterapia basados en taxanos. Los resultados evaluados incluyen, además del dolor, otros signos neuropáticos y su influencia en las actividades de la vida diaria. Los estudios variaron en términos de intervención y fase de tratamiento. Sólo uno de los estudios demostró un resultado significativamente positivo a favor del grupo de intervención. Conclusión: Los estudios clínicos aleatorizados aportan escasa evidencia sobre los efectos positivos de la intervención fisioterapéutica sobre el dolor neuropático periférico inducido por los tratamientos del cáncer de mama.
Palabras clave: Manejo del Dolor/métodos; Polineuropatía; Neoplasias de la Mama. Antineoplásicos/farmacología; Modalidades de Fisioterapia.
INTRODUÇÃO
O câncer é um problema de saúde pública mundial e, especificamente, o de mama é o mais prevalente entre as mulheres de todas as idades em todo mundo1. No Brasil, a alta incidência na população feminina se mantém; afora os tumores de pele não melanoma, o câncer de mama ocupa a primeira posição mais frequente em todas as Regiões brasileiras2. Nas últimas décadas, avanços significativos foram observados em técnicas diagnósticas, tratamento e cuidados no universo oncológico. Apesar de tais avanços terem resultado em um aumento da taxa de sobrevivência, estabeleceram-se novos desafios para o sistema de saúde, no que concerne à reabilitação ideal a longo prazo e apoio integral a essas pacientes. Entende-se como sobrevivência ao câncer o estado que se inicia no dia do diagnóstico e continua até o fim da vida. Três fases podem ser reconhecidas: (1) sobrevida aguda – estádio inicial ou tempo durante o tratamento e a cura; (2) sobrevida permanente – conviver com o câncer; e (3) sobrevida estendida – curado, mas não livre de sofrimento relacionado. Na fase estendida, é constante o relato de sintomas que surgem e/ou persistem para além da conclusão do tratamento, uma importante população que necessita de reabilitação3.
Em suma, os tratamentos para o câncer de mama são multimodais, introduzidos de modo neoadjuvante ou adjuvante, combinam terapias locais, ou seja, cirurgias e radiação, com terapias sistêmicas, as quais incluem uma ampla gama de medicamentos, entre quimioterapia e terapia-alvo molecular, podendo ser administradas isoladamente ou em regimes de múltiplas drogas4. As condutas terapêuticas utilizadas objetivam primariamente erradicar a doença e/ou aumentar as chances de sobrevivência, todavia, ao mesmo tempo em que a evolução no diagnóstico, o tratamento e os cuidados alcançaram tais objetivos, as características heterogêneas e agressivas dos tratamentos contra o câncer levam a efeitos colaterais importantes, estabelecendo assim novos desafios para o sistema de saúde. Tornou-se, então, essencial uma assistência para reabilitação a longo prazo, uma vez que pacientes submetidas ao tratamento frequentemente relatam dor, em especial de caráter crônico, linfedema, fadiga e depressão, culminando na redução da qualidade de vida relacionada à saúde (QVRS)³.
Estima-se que até 50% das pacientes submetidas a tais terapias sofrerão com a dor crônica com componente neuropático, induzida por danos intraoperatórios às estruturas do sistema nervoso ou após radioterapia e/ou quimioterapia5. As síndromes neuropáticas, nesse contexto, apresentam três subdivisões que serão abordadas neste estudo: polineuropatia crônica dolorosa induzida por quimioterapia (PCDQ); neuropatia crônica dolorosa induzida por radiação (NCDR); dor crônica pós-cirúrgica (DCPC)6. A PCDQ é observada em 90% dos pacientes expostos aos agentes neurotóxicos quimioterápicos. Em sincronicidade, a dor crônica de natureza neuropática é predominante após os procedimentos cirúrgicos no câncer de mama7.
Muitas diretrizes são estabelecidas mundialmente para o manejo da dor crônica e, cada vez mais, estuda-se a respeito desse quadro no universo do câncer. Apesar disso, a dor crônica permanece pouco reconhecida e subtratada na fase de sobrevivência estendida no câncer de mama. Alguns fatores podem ser atribuídos a essa realidade, entre eles, a crença dos pacientes de que a dor é inevitável, fazendo com que a dor não seja relatada aos profissionais da saúde; a avaliação da dor realizada de forma pobre pelo profissional; a não adesão dos pacientes ao tratamento, muitas vezes por equívocos na intervenção medicamentosa; ou ainda, conhecimento e/ou confiança subótima do profissional de saúde na aplicação de diretrizes de manejo da dor crônica. Não menos importante, a subinformação e a falta de educação em saúde impedem que sobreviventes do câncer procurem apoio quando necessário e conheçam as possibilidades para alívio da dor.
Para tanto, pensando na atuação do profissional fisioterapeuta, seu papel na reabilitação oncológica e sua íntima relação com o manejo da dor humana, propõe-se o estudo dos efeitos das modalidades fisioterapêuticas como uma alternativa de intervenção na dor neuropática decorrente das terapias utilizadas contra o câncer de mama. O objetivo é revisar quais as modalidades fisioterapêuticas são utilizadas no manejo e seus efeitos na dor neuropática periférica decorrente das terapias integrativas utilizadas no tratamento do câncer de mama.
MÉTODO
A questão de investigação foi formulada de acordo com o acrônimo PICO (população, intervenção, comparação, desfecho), conforme as diretrizes do Preferred Reporting Items for Systematic review and Meta-Analysis Protocols (PRISMA-P)8. Demais passos para a elaboração do protocolo de pesquisa seguiram as mesmas diretrizes. Este estudo foi registrado na base de revisões sistemáticas do International Prospective Register of Systematic Reviews (PROSPERO9) com ID CRD42023382715.
A seguinte combinação de descritores foi então utilizada como estratégia de busca “chronic cancer treatment pain AND neuralgia OR neuropathic pain OR painful peripheral neuropathy AND breast cancer OR breast neoplasms AND pain management AND physical therapy”, a qual foi realizada nas bases de dados MEDLINE via portal PubMed e Cochrane Library. Concomitante à estratégia de busca utilizada nas referidas bases, foram aplicados os filtros metodológicos, restringindo a busca a ensaios clínicos, e temporal, que delimitou os resultados em publicações feitas a partir de 2017. O período de busca compreendeu setembro de 2022 a julho de 2023.
Para contemplar as evidências relevantes, foram incluídos ensaios clínicos randomizados, publicados na língua inglesa, cegos e não cegos, para terapeuta e participantes, visto a natureza e o momento das intervenções de escolha. A população do estudo foi de mulheres adultas, já submetidas ou em tratamento oncológico para o câncer de mama, por procedimentos cirúrgicos, quimioterapia ou radioterapia, neoadjuvante ou adjuvante, que descrevessem dor por neuropatia induzida pelo tratamento. Excluíram-se aquelas com dor provocada pelo câncer propriamente dito, por compressão ou infiltração do sistema nervoso central ou periférico; ou por comorbidades. Quanto à intervenção, incluíram-se estudos que avaliaram modalidades específicas da fisioterapia no manejo da dor neuropática periférica decorrente do tratamento oncológico contra o câncer de mama. Isso abrange estudos que usaram técnicas pertinentes às especialidades da fisioterapia reconhecidas pelo Conselho Federal de Fisioterapia e Terapia Ocupacional (Coffito). Para o momento de intervenção, foram considerados estudos realizados para prevenção ou para gerenciamento dos sintomas, antes, durante e após a finalização do tratamento oncológico. Estudos que avaliassem outras terapias de modo concomitante à intervenção da fisioterapia foram excluídos.
A extração de dados foi realizada por um revisor utilizando um formulário padronizado com as seguintes informações de cada estudo: (a) pesquisador que realizou a extração; (b) data da extração; (c) elementos de identificação; (d) objetivos; (e) desenho do estudo; (f) critérios de elegibilidade; (g) participantes; (h) descrição da intervenção utilizada; (i) resultados. A qualidade dos estudos foi avaliada pela ferramenta de risco de viés da Cochrane para estudos randomizados versão atualizada (Cochrane risk-of-bias tool for randomized trials - RoB 2)10 e relatada posteriormente na seção de resultados.
A síntese envolveu a combinação e o resumo dos resultados individuais de cada estudo incluído, por uma abordagem narrativa, na qual foram avaliados, além dos resultados, metodologia, consistências e inconsistências entre os estudos e correlação com a literatura prévia. Para o fechamento da síntese, a pergunta de pesquisa foi retomada.
RESULTADOS
A estratégia de busca utilizada encontrou 1.871 artigos correspondentes na base de dados Cochrane Library e 33 no portal PubMed, totalizando 1.904 estudos disponíveis para triagem. Foram excluídas 132 duplicatas, restando 1.772 estudos a serem considerados. A partir desse número, quatro artigos foram removidos por não estarem no idioma adequado. Subsequentemente, a seleção se deu pela leitura do título e do resumo, sendo removidos 1.693 artigos que não corresponderam ao tema ou à metodologia buscadas; 39 que não atendiam aos principais critérios de caracterização da população e intervenção ou desfecho estudados, e 26 que não estavam disponíveis na íntegra, sem contato com o autor correspondente. Por fim, dez artigos foram examinados em texto completo, seis destes não atenderam aos critérios de inclusão, resultando em quatro estudos elegíveis para esta revisão. O fluxograma que descreve o processo de seleção realizado está apresentado na Figura 1.
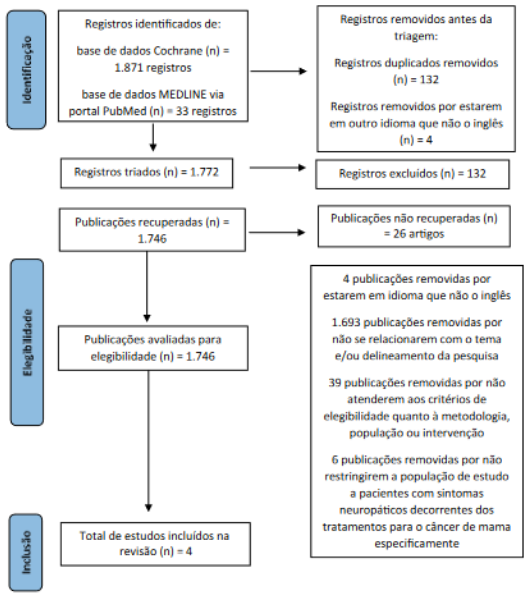
Figura 1. Fluxograma da triagem de estudos
Fonte: Adaptado de PRISMA8.
Uma síntese das informações extraídas de cada um dos quatro estudos que preencheram todos os critérios de inclusão para esta revisão está descrita no Quadro 1. Os estudos variam especialmente quanto à intervenção de escolha e ao momento com caráter preventivo ou curativo de gerenciamento. Apenas um estudo aborda outras terapias oncológicas que não a intervenção cirúrgica e a quimioterapia. Todos os ensaios inclusos apontam os efeitos deletérios advindos de um regime quimioterápico por taxanos que pode ser adjuvante ou neoadjuvante; do mesmo modo, apresentam diversos pontos de avaliação ao longo do período de intervenção. Todas as intervenções de escolha apontam alguma especialidade da fisioterapia, incluindo cinesioterapia, termoterapia e terapia manual.
Quadro 1. Extração de dados dos artigos selecionados para revisão
Legendas: GC = grupo controle; GI = grupo intervenção; BPI = brief pain inventory; CAMP = compound muscle action potential; DASH = disabilities of the arm, shoulder, and hand; EORTC QLQ CIPN20 = european organization for research and treatment of cancer-quality of life questionnaire for chemotherapy-induced peripheral neuropathy; NCS = nerve conduction studies; NPSI = neuropathic pain symptom inventory; QST = quantitative sensory testing; RM = repetições máximas; S-LANSS = Leeds assessment of neuropathic symptoms and signs; SNAP = sensory nerve action potential.
A possibilidade de viés entre os estudos considerados se deu pela ferramenta Cochrane para risco de viés Rob 210. Os itens foram avaliados subjetivamente por dois revisores de forma independente, resultando na inclusão de todos os artigos previamente selecionados, visto a aspiração em reunir todas as evidências disponíveis na literatura. Majoritariamente, a natureza das intervenções impossibilitou a realização de ensaios duplo-cegos. Eventuais discordâncias entre os revisores foram resolvidas em reunião de consenso. Um resumo dos riscos de viés dos estudos incluídos encontra-se na Figura 2.
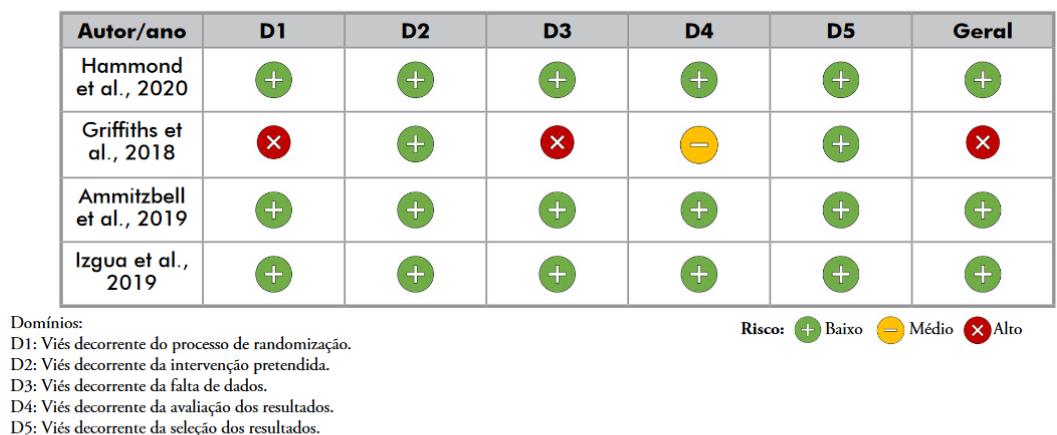
Figura 2. Avaliação do risco de viés dos estudos considerados para revisão
DISCUSSÃO
Ao revisar os mecanismos e os métodos de detecção da dor neuropática periférica induzida pelo tratamento do câncer de mama e efeitos das modalidades fisioterapêuticas no manejo dessa dor, este estudo tem como objetivo reunir as evidências clínicas que possam contribuir para a atuação da equipe multiprofissional, em especial fisioterapeutas que irão trabalhar no manejo e gerenciamento da dor entre essas pacientes. Foram incluídos um total de quatro ensaios clínicos randomizados que propuseram diferentes métodos de intervenção utilizadas como técnicas fisioterapêuticas, entre elas a cinesioterapia incorporada a um programa de exercícios domiciliares, um programa de treino resistido com progressão de cargas, a termoterapia por meio da crioterapia e a terapia manual com a massagem clássica como método preventivo. Diferentes intervenções podem apresentar benefícios na melhora da dor, da função, e na QVRS como uma alternativa viável para a neuropatia periférica induzida pelo tratamento oncológico. Até o momento, esta é a primeira revisão sistemática de literatura a relatar acerca da intervenção da fisioterapia para neuropatia periférica em pacientes com câncer de mama.
Predominantemente, as amostras dos presentes ensaios estavam sob regimes quimioterápicos à base de taxanos (p. ex. paclitaxel e docetaxel). Atualmente, esse é o regime de quimioterapia de primeira linha usado no tratamento para o câncer de mama tanto em estádios iniciais como avançados e metastáticos, atua prevenindo o crescimento tumoral por meio de mecanismos de estabilização de microtúbulos celulares. Contudo, a alta neurotoxicidade está associada à redução da dose administrada e, algumas vezes, à descontinuidade do tratamento, tornando maior o risco de morbimortalidade entre as pacientes. A neuropatia periférica induzida pela quimioterapia (NPIQ) é o principal efeito adverso dose-limitante entre taxanos, com prevalência estimada em até 81%10. Desenvolve-se em mãos e pés, afetando fibras nervosas Aβ, Aδ e fibras C, as quais envolvem percepção e condução sensorial de toque, vibração, detecção térmica e de dor, e, consequentemente, resultando em sintomas neuropáticos clássicos que incluem a hipoestesia, a hiperalgesia, a alodinia e a dor neuropática12.
Hammond et al.12 avaliaram os efeitos de um programa de fisioterapia na prevenção e manejo pós-regime quimioterápico da NPIQ. Os resultados obtidos não demonstraram significância estatística, porém todos indicaram um movimento unilateral de melhoria nos escores obtidos pelos pacientes do grupo intervenção, além disso, observaram também a associação entre a prática de atividade física moderada (120 minutos/semana) e a preservação sensorial. Apesar de este não ter sido um resultado controlado e randomizado, corrobora outros estudos presentes na literatura, os quais descrevem os efeitos do exercício físico na neuromodulação da dor por dano neural. Em revisão sistemática, Zhang et al.13 reuniram um total de oito revisões sistemáticas e 21 ensaios clínicos, os quais avaliaram diferentes modalidades de exercícios, entre alongamentos, treinos resistidos, treinos aeróbicos, exercícios aquáticos e proprioceptivos, utilizados no manejo da neuropatia de diferentes etiologias, entre elas a induzida por quimioterapia, e concluíram que o exercício físico pode ser considerado uma alternativa viável e eficaz no tratamento da neuropatia periférica. Nesse mesmo estudo, a mobilização neural de membros superiores foi a técnica fisioterapêutica utilizada.
A mobilização neural é uma técnica não invasiva que tem sido demonstrada clinicamente efetiva na redução da dor. Essa técnica visa restaurar a mobilidade e elasticidade do sistema nervoso periférico e, assim, proporcionar melhores condições homeostáticas na presença de dano neural. Todavia, mais estudos são necessários para compor uma base de dados e ensaios com humanos. Em estudo de modelo animal, Santos et al.14 sugeriram a ativação de vias endógenas ativadas pela modulação neural da dor por meio da técnica, confirmando hipótese inicial de que a analgesia por técnicas não invasivas se dá por mecanismos neuronais centrais, sendo os opiáceos endógenos e os mecanismos inibitórios descendentes os mais reconhecidos.
Hoje o manejo das neuropatias periféricas, com ênfase para a dor neuropática, objetiva controlar ou amenizar os sintomas, visto a dificuldade em tratar o dano nervoso diretamente. Inúmeras opções farmacológicas estão disponíveis como tratamento, entretanto, permanecem apresentando baixa eficácia e muitos efeitos adversos, anticolinérgicos ou relacionados ao uso e dependência de opioides, assim, abordagens alternativas, como o exercício físico terapêutico, ganham cada vez mais atenção da equipe de saúde. Nesse âmbito, a fisioterapia pode atuar em uma gama de opções terapêuticas associadas à mobilização, alongamentos, e exercícios resistidos e aeróbicos15.
Harmônico a esse cenário, Ammitzbel et al.16 investigaram o efeito do treinamento resistido progressivo sobre a dor em regime pós-operatório, considerando que métodos distintos para o exercício, diferentes intensidades e frequência de treino podem produzir diferentes efeitos. Anteriormente, a ação do treino resistido foi avaliado para outros desfechos, se mostrando útil na reabilitação de força e função após procedimentos cirúrgicos para determinados cânceres de mama. Nesse estudo, os resultados não mostraram efeitos estatisticamente significativos. Contudo, as avaliações realizadas apontaram para um efeito de controle da dor, favorecendo o grupo intervenção para todos os desfechos contínuos analisados: dor, dor neuropática e influência da dor em seis aspectos da vida diária. A hipótese desses autores é a existência de um subgrupo não identificado no qual o treinamento resistido seja mais eficaz, como, por exemplo, mulheres sedentárias com relato de dor pós-operatória. Além disso, o estudo apresenta limitações quanto ao poder de detectar diferenças suficientes na avaliação da dor, uma vez que a dor e a dor neuropática não foram desfechos primários analisados. Em ensaio clínico randomizado realizado por Dhawan et al.15, com uma amostra de 45 pacientes com câncer recebendo terapia adjuvante com paclitaxel, observou-se que um treino domiciliar de força e equilíbrio é capaz de reduzir dor neuropática por NPIQ e melhorar a QVRS. Nesse estudo, foram utilizados escores de dor neuropática avaliada pelo questionário Leeds assessment of neuropathic symptoms and signs (S-LANSS).
Ambos os estudos acerca dos efeitos do exercício físico no manejo da neuropatia apresentaram limitações quanto ao número de variáveis estudadas e prioridade do desfecho dor, as quais podem ter sugestionado os resultados em termos estatísticos. Não obstante, a literatura traz, em estudos com amostra e intervenção, similares resultados com relevância estatística. Outro ponto a ser levantado diz respeito ao método de autoadministração do programa de exercícios e educação em saúde trazida pelo profissional da equipe de saúde, salientando que, apesar de autoadministrado, ainda assim, é reavaliado pelo profissional capacitado. Proporcionar informações claras e orientações sobre a condição do paciente é crucial. Educar sobre o manejo da dor não se resume apenas a fornecer conhecimento, envolve ainda promover mudanças comportamentais e desafiar crenças limitantes. Essas ações não apenas ajudam a aliviar a angústia, medo e ansiedade17, já significativos para a maioria dos pacientes com câncer, mas também contribuem para uma melhor qualidade de vida. Trazer autonomia e maior segurança ao paciente pode interferir positivamente perante a ação do sistema límbico sobre a via dolorosa e, como muito visto em prática clínica, o comportamento positivo por parte do paciente pode influenciar substancialmente no engajamento ao tratamento.
Seguindo as modalidades terapêuticas revisadas, a crioterapia é uma das técnicas amplamente utilizadas na fisioterapia como parte da termoterapia, trata-se da aplicação superficial de frio como agente terapêutico, comumente utilizada no alívio da dor. A aplicação se dá em áreas específicas por meio de aplicação local ou mais amplamente por aplicativos não locais. A inflamação crônica, mediada pela estimulação química e mecânica das terminações nervosas, tem papel importante na perpetuação da dor frente a um dano, inclusive em nível neural, o que justifica o uso da crioterapia para reduzir a inflamação em dores crônicas. Evidências sugerem que a crioterapia diminui a inflamação reduzindo a ação de citocinas pró-inflamatórias TNF-α e propiciando a ação anti-inflamatória mediada por interleucina-10 (IL-10) e interleucina-6 (IL-6), a qual recentemente sugeriu-se também apresentar propriedades anti-inflamatórias. Outro mecanismo proposto para ação do frio como meio terapêutico é sobre a velocidade de condução nervosa das vias de dor; estudos trazem uma redução considerável na latência de transmissão tanto em vias motoras quanto sensoriais, resultando no aumento do limiar da dor. E, por fim, a crioterapia está também associada à redução do estresse oxidativo18.
Griffiths19 realizou ensaio clínico randomizado para avaliar a eficácia da crioterapia na prevenção da neuropatia periférica induzida por paclitaxel. Tal estudo apresentou limitações metodológicas importantes. A amostra sofreu com variações significativas durante os pontos de avaliação, inicialmente com n = 29; após 22 desistências, o n final foi de apenas sete participantes. Desse modo, as avaliações estatísticas dos resultados foram influenciadas, e o estudo foi incapaz de demonstrar benefício da crioterapia para prevenção da neuropatia induzida por paclitaxel. Os autores atribuíram os resultados pelo menos em parte à alta taxa de desistência, mas também à impossibilidade de cegar as participantes, em virtude da natureza dos equipamentos utilizados (peças de histogel), o que pode afetar as respostas aos questionários autorrelatados, como neuropathic pain symptom inventory (NPSI), brief pain inventory (BPI) e quantitative sensory testing (QST).
A desistência relacionada ao desconforto na intervenção, a necessidade de investimentos adicionais por parte da equipe oncológica, no que diz respeito à instalação de freezers, e a equipe responsável para controlar tempo e a temperatura de preparo das peças trouxeram o questionamento quanto à viabilidade da terapia, ao mesmo tempo em que o tamanho final da amostra impossibilitou a compreensão quanto aos possíveis benefícios da terapia. Considerando o amplo tempo de aplicação utilizado para essa intervenção, existe a hipótese de que a redução desse tempo pode reduzir o abandono por parte das participantes.
Izgua et al.20 investigaram o efeito da massagem clássica como prevenção da neuropatia periférica induzida por quimioterapia em pacientes com câncer de mama recebendo paclitaxel. Os pesquisadores constataram que a massagem contribui para o controle dos sintomas neuropáticos, de modo que, após 12 sessões de massagem clássica, os pacientes com dor neuropática periférica aumentarem os escores no grupo controle, enquanto no grupo intervenção não houve alterações a partir da linha de base, sendo os resultados apresentados estatisticamente significantes. Mais ensaios randomizados e controlados realizados em humanos são necessários para suportar os achados e contribuir com a literatura existente. Evidências quanto aos mecanismos de analgesia da técnica são trazidos em modelos animais. Segundo Chimenti; Frey-Law; Sluka17, demonstrou-se em modelos animais de dor neuropática que a terapia manual promove condições propícias para a cicatrização, aumentando a espessura da bainha de mielina em nervos periféricos lesados, além de reduzir a compressão nervosa. Analogamente, também em modelo animal, Wang et al.21 trazem os efeitos da massagem sobre o toll-like receptor 4 (TLR4), um tipo de receptor que atua na transdução da resposta imune e identifica moléculas padrão relacionadas à patogenicidade, com desempenho importante na mediação da dor neuropática, sendo que a massagem pode inibir a sinalização TLR4 e reduzir os fatores inflamatórios, podendo ser um mecanismo válido no alívio da dor neuropática.
No estudo conduzido por Izgua et al.20, a massagem clássica sueca é trazida como uma das técnicas utilizada pela equipe de enfermagem. Considerando o modelo multiprofissional na assistência e natureza da técnica, o fisioterapeuta, como profissional habilitado para o uso de terapias manuais, caracterizado em especial pelo uso das mãos como uma de suas ferramentas terapêuticas, bem como com possibilidade de habilitação específica em fisioterapia oncológica, pode ser designado para a prática da técnica, levando em conta a assistência profissional adequada e específica, que atenda às exigências clínico-cinesiológico-funcionais dos pacientes oncológicos, em especial aqueles sofrendo por efeitos deletérios dos tratamentos a que foram submetidos.
A fisioterapia propõe uma pluralidade abrangente em alternativas não farmacológicas que podem atuar na prevenção, gerenciamento e manejo da neuropatia periférica. Notavelmente, o exercício físico terapêutico, com uso da cinesioterapia, ostenta efeitos importantes sobre a neuromodulação da dor neuropática, além de operar em outros aspectos biopsicossociais relacionados à dor crônica, especialmente quanto à QVRS. Posto isso, ao levar em conta a possível contribuição do fisioterapeuta no amparo dessa população, poucos estudos foram elegíveis para esta revisão. Um dos desafios encontrados ao longo da triagem refere-se à restrição da análise dos resultados para mulheres tratadas para o câncer de mama, em razão de grande parte dos estudos não poder ser incluída pela característica mista da população. A escolha da delimitação amostral para pacientes com câncer de mama se deu, em princípio, pela alta incidência e prevalência da malignidade na população feminina, além de propiciar uma análise mais precisa acerca dos efeitos das intervenções de escolha, ponderando os agentes antineoplásicos específicos utilizados. Ademais, não foi realizada busca manual nem consulta à lista de referências que poderia identificar estudos potencialmente elegíveis para a revisão. Por fim, pode haver viés da língua, uma vez que, por não estarem em inglês, quatro artigos acabaram sendo excluídos considerando a dificuldade de análise e compreensão.
CONCLUSÃO
Os resultados do efeito da fisioterapia no manejo e gerenciamento da neuropatia periférica induzida pelos tratamentos oncológicos para o câncer de mama são escassos, e, na maioria dos estudos avaliados, não houve diferenças significativas entre os grupos de tratamento e controle. Essa escassez de resultados pode ser relacionada ao número limitado de estudos aqui revisados, visto a dificuldade em encontrar ensaios clínicos realizados com exclusividade na população-alvo. Ponderando a singularidade das condutas intervencionais em cada tipo de câncer, sugere-se a produção de mais ensaios clínicos randomizados que avaliem populações oncológicas específicas. Concomitantemente, destacam-se a necessidade e a importância de atualizações constantes quanto à fisiopatologia, aos protocolos e às intervenções com base em ensaios clínicos randomizados, bem como a avaliação da aderência e efeitos adversos para o embasamento consciente e criterioso das evidências atuais na tomada de decisões sobre o cuidado individual do paciente.
CONTRIBUIÇÕES
Julia Formentini Viesser, Caroline Helena Lazzarotto de Lima e Mariana Zancan contribuíram substancialmente na concepção e/ou no planejamento do estudo; na obtenção, análise e interpretação dos dados; na redação e revisão crítica e aprovaram a versão final a ser publicada.
DECLARAÇÃO DE CONFLITO DE INTERESSES
Nada a declarar.
FONTES DE FINANCIAMENTO
Não há.
REFERÊNCIAS
1. Hauth F, De-Colle C, Weidner N, et al. Quality of life and fatigue before and after radiotherapy in breast cancer patients. Strahlenther Onkol. 2021;197(4):281-7. doi: https://doi.org/10.1007/s00066-020-01700-1
2. Santos MO, Lima FCS, Martins LFL, et al. Estimativa de incidência de câncer no brasil, 2023-2025. Rev Bras Cancerol. 2023;69(1):e-213700. doi: https://doi.org/10.32635/2176-9745.RBC.2023v69n1.3700
3. Olsson Möller U, Beck I, Rydén L, et al. A comprehensive approach to rehabilitation interventions following breast cancer treatment - a systematic review of systematic reviews. BMC Cancer. 2019;19(1):472. doi: https://doi.org/10.1186%2Fs12885-019-5648-7
4. Shien T, Iwata H. Adjuvant and neoadjuvant therapy for breast cancer. JPN J Clin Oncol. 2020;50(3):225-9. doi: https://doi.org/10.1093/jjco/hyz213
5. Fontes F, Gonçalves M, Pereira S, et al. Neuropathic pain after breast cancer treatment and its impact on sleep quality one year after cancer diagnosis. Breast. 2017;33:125-31 doi https://doi.org/10.1016/j.breast.2017.03.013
6. Ilhan E, Chee E, Hush J, et al. The prevalence of neuropathic pain is high after treatment for breast cancer: a systematic review. Pain. 2017;158(11):2082-91. doi: https://doi.org/10.1097/j.pain.0000000000001004
7. Leysen L, Adriaenssens N, Nijs J, et al. Chronic pain in breast cancer survivors: nociceptive, neuropathic, or central sensitization pain? Pain Pract. 2019;19(2):1983-5. doi: https://doi.org/10.1111/papr.12732
8. Page MJ, McKenzie JE, Bossuyt PM, et al. A declaração PRISMA 2020: diretriz atualizada para relatar revisões sistemáticas. Rev Panam Salud Publica. 2022;46:e112. doi: https://doi.org/10.26633%2FRPSP.2022.112
9. University of York. Centre for Reviews and Dissemination. York: University of York; 2019. PROSPERO - International prospective register of systematic reviews. 2023. [acesso 2023 ago 31]. Disponível em: https://www.crd.york.ac.uk/PROSPERO/
10. RoB 2: Risk of Bias 2 [Internet]. Versão 5. [Copenhagen]: Cochrane Denmark; 2011. [acesso 2023 mar 9]. Disponível em: https://www.riskofbias.info/
11. Guijosa A, Freyria A, Espinosa-Fernandez Jr, et al. Pharmacogenetics of taxane-induced neurotoxicity in breast cancer: systematic review and meta-analysis. Clin Transl Sci. 2022;15(10):2403-36. doi: https://doi.org/10.1111%2Fcts.13370
12. Hammond EA, Pitz M, Shay B. Neuropathic pain in taxane-induced peripheral neuropathy: evidence for exercise in treatment. Neurorehabil Neural Repair. 2019;33(10):792-9. doi: https://doi.org/10.1177/1545968319860486
13. Zhang YH, Hu HY, Xiong YC, et al. Exercise for neuropathic pain: a systematic review and expert consensus. Front Med (Lausanne). 2021;24(8). doi: https://doi.org/10.3389%2Ffmed.2021.756940
14. Santos FM, Grecco LH, Pereira MG, et al. The neural mobilization technique modulates the expression of endogenous opioids in the periaqueductal gray and improves muscle strength and mobility in rats with neuropathic pain. Behav Brain Funct. 2014;19(19). doi: https://doi.org/10.1186%2F1744-9081-10-19
15. Dhawan S, Andrews R, Kumar L, et al. A randomized controlled trial to assess the effectiveness of muscle strengthening and balancing exercises on chemotherapy-induced peripheral neuropathic pain and quality of life among cancer patients. Cancer Nurs. 2020;43(4):269-80. doi: https://doi.org/10.1097/ncc.0000000000000693
16. Ammitzbel G, Andersen KG, Bidstrup PE, et al. Effect of progressive resistance training on persistent pain after axillary dissection in breast cancer: a randomized controlled trial. Breast Cancer Res Treat. 2019;179(1):173-83. doi: https://doi.org/10.1007/s10549-019-05461-z
17. Chimenti RL, Frey-Law LA, Sluka KA. A mechanism-based approach to physical therapist management of pain. Phys Ther. 2018;98(5):302-14. doi: https://doi.org/10.1093%2Fptj%2Fpzy030
18. Garcia C, Karri J, Zacharias NA, et al. Use of cryotherapy for managing chronic pain: an evidence-based narrative. Pain Ther. 2021;10(1):81-100. doi: https://doi.org/10.1007%2Fs40122-020-00225-w
19. Griffiths C, Kwon N, Beaumont JL, et al. Cold therapy to prevent paclitaxel-induced peripheral neuropathy. Support Care Cancer. 2018;26:3461-9. doi: https://doi.org/10.1007/s00520-018-4199-9
20. Izgua N, Metin ZG, Karadas C, et al. “Prevention of chemotherapy-Induced peripheral neuropathy with classical massage in breast cancer patients receiving paclitaxel: an assessor-blinded randomized controlled trial.” Eur j oncol nurs. 2019;40:36-43, doi: https://doi.org/10.1016/j.ejon.2019.03.002
21. Wang Q, Lin J, Yang P, et al. Effect of massage on the tlr4 signalling pathway in rats with neuropathic pain. Pain Res Manag. 2020;2020:8309745. doi: https://doi.org/10.1155%2F2020%2F8309745
Recebido em 12/9/2023
Aprovado em 1/2/2024
Editor-associado: Fernando Lopes Tavares de Lima. Orcid iD: https://orcid.org/0000-0002-8618-7608
Editora-científica: Anke Bergmann. Orcid iD: https://orcid.org/0000-0002-1972-8777
![]()
Este é um artigo publicado em acesso aberto (Open Access) sob a licença Creative Commons Attribution, que permite uso, distribuição e reprodução em qualquer meio, sem restrições, desde que o trabalho original seja corretamente citado.