ARTIGO ORIGINAL
Análise da Sobrevida de Pacientes Submetidos a Transplante Alogênico de Células Progenitoras Hematopoiéticas na Pré e na Pandemia de Covid-19 em um Hospital do Rio de Janeiro
Analysis of the survival of patients undergoing Allogeneic Hematopoietic Progenitor Cell Transplantation before and during the COVID-19 Pandemic in a Hospital in Rio de Janeiro
Análisis de la Supervivencia de Pacientes Sometidos a Trasplante Alogénico de Células Progenitoras Hematopoyéticas antes y durante la Pandemia de COVID-19 en un Hospital de Río de Janeiro
https://doi.org/10.32635/2176-9745.RBC.2024v70n3.4733
Pedro Felipe Couto Vieira1; Jackeline Christiane Pinto Lobato2; Carla Cristina Pedrosa de Lira de Morais3; Rômulo Gonçalves Galvani4; Marina Vieira Agostinho Pereira5; Amanda de Moura Souza6
1Instituto Nacional de Câncer (INCA), Centro de Transplante de Medula Óssea (Cemo), Banco de Sangue de Cordão Umbilical e Placentário. Rio de Janeiro (RJ), Brasil. E-mail: pedro.vieira@inca.gov.br. Orcid iD:
2Universidade Federal Fluminense, Instituto de Saúde Coletiva, Departamento de Epidemiologia e Bioestatística. Niterói (RJ), Brasil. E-mail: jackie.lobato@gmail.com. Orcid iD: https://orcid.org/0000-0003-3845-959X
3INCA, Cemo, Centro de Processamento Celular. Rio de Janeiro (RJ), Brasil. E-mail: cpliramorais@gmail.com. Orcid iD: orcid.org/0000-0003-0553-7272
4,5Fundação Oswaldo Cruz, Instituto Oswaldo Cruz, Laboratório de Pesquisa sobre o Timo. Rio de Janeiro (RJ), Brasil. E-mails: romulo.galvani@ufrj.br; marinavap@gmail.com. Orcid iD: orcid.org/0000-0002-2946-375X; Orcid iD: https://orcid.org/0000-0001-8665-0554
6Universidade Federal do Rio de Janeiro, Instituto de Estudos em Saúde Coletiva. Rio de Janeiro (RJ), Brasil. E-mail: amandamoura@iesc.ufrj.br. Orcid iD: https://orcid.org/0000-0002-8962-798X
Endereço para correspondência: Pedro Felipe Couto Vieira. Cemo/INCA. Praça Cruz Vermelha, 23 – Centro. Rio de Janeiro (RJ), Brasil. CEP 20230-130. E-mail: pedro.vieira@inca.gov.br
RESUMO
Introdução: A pandemia de covid-19 alterou a dinâmica de conservação dos
enxertos e de realização dos transplantes de células progenitoras hematopoiéticas
(TCPH) alogênicos, o que pode ter afetado a sobrevida dos pacientes. Objetivo: Analisar a sobrevida dos pacientes
pós-TCPH imediato (100 dias pós-TCPH) segundo a exposição aos diferentes tipos de
transplantes e fontes de enxerto, na pré-pandemia e na pandemia de covid-19. Método:
Estudo de coorte retrospectivo de base hospitalar com 246 pacientes que realizaram
TCPH em hospital de referência no município do Rio de Janeiro entre janeiro/2016
e dezembro/2021. Os métodos de log-rank e
Kaplan-Meier foram utilizados para estimar as funções de sobrevida de pós-TCPH
imediato. Resultados: A taxa de mortalidade foi ligeiramente superior na
pandemia quando comparada à pré-pandemia (10,1% vs. 8,8%). O enxerto mais
utilizado em todo o período estudado foi medula óssea (MO) com 85%. Porém, na pandemia,
50,5% das coletas alogênicas foram realizadas utilizando o sangue periférico mobilizado
(SPM). Oito por cento dos enxertos criopreservados não foram infundidos. Não foram
observadas diferenças na sobrevida entre pacientes que utilizaram SPM como fonte
de enxerto em relação à MO. Conclusão: Os tipos de enxerto e as fontes de
transplantes não influenciaram a sobrevida dos pacientes em ambos os períodos. A
criopreservação se apresentou como uma ferramenta importante para superar os desafios
logísticos ligados à pandemia de covid-19, porém, um percentual relevante de enxertos
criopreservados não foi utilizado. Assim, é necessário que os centros transplantadores
voltem a realizar TCPH com produtos frescos, reduzindo o percentual de inutilização
dos enxertos.
Palavras-chave: COVID-19; Transplante de Medula Óssea; Criopreservação; Sobrevida.
ABSTRACT
Introduction: The COVID-19 pandemic has changed the dynamics of graft conservation and performance of allogeneic hematopoietic progenitor cell transplantation (HPCT), which may have affected patient survival. Objective: To analyze the survival of patients after immediate post-HPCT (100 days after HPCT) according to exposure to different types of transplants and graft sources, before and during the COVID-19 pandemic. Method: Hospital-based retrospective cohort study with 246 patients who underwent HPCT at a referral hospital in the city of Rio de Janeiro between January 2016 and December 2021. The log-rank and Kaplan-Meier methods were used to estimate the survival functions of immediate post-HPCT. Results: The mortality rate was slightly higher during the pandemic when compared to pre-pandemic (10.1% vs. 8.8%). The graft most utilized throughout the period investigated was bone marrow (BM, 85%). However, during the pandemic, 50.5% of allogeneic collections were performed using mobilized peripheral blood (MPB). Eight percent of cryopreserved grafts were not infused. No differences in survival were observed among patients who used MPB as a graft source compared to BM. Conclusion: Graft types and transplant sources did not influence patient survival in either period. Cryopreservation proved to be an important tool to overcome the logistical challenges associated with the COVID-19 pandemic, however, a relevant percentage of cryopreserved grafts were not used. Therefore, transplantation centers should resume HPCT with fresh products, reducing the percentage of grafts unused.
Key words: COVID-19; Bone Marrow Transplant; Cryopreservation; Survival.
RESUMEN
Introducción: La pandemia de COVID-19 cambió la dinámica de conservación del injerto y la realización de trasplantes alogénicos de células progenitoras hematopoyéticas (TCPH), lo que puede haber afectado la supervivencia de los pacientes. Objetivo: Analizar la supervivencia de los pacientes inmediatamente después del TCPH (100 días después del TCMH) según la exposición a diferentes tipos de trasplantes y fuentes de injerto, antes de la pandemia y durante la pandemia de COVID-19. Método: Estudio de cohorte retrospectivo hospitalario con 246 pacientes sometidos a TCPH en un hospital de referencia de la ciudad de Río de Janeiro entre enero/2016 y diciembre/2021. Se utilizaron los métodos log-rank y Kaplan-Meier para estimar las funciones de supervivencia inmediatas post-TCPH. Resultados: La tasa de mortalidad fue ligeramente mayor durante la pandemia en comparación con la prepandemia (10,1% vs. 8,8%). El injerto más utilizado durante todo el periodo estudiado fue el de médula ósea (MO, 85%). Sin embargo, durante la pandemia, el 50,5% de las recolecciones alogénicas se realizaron utilizando la sangre periférica movilizada (SPM). El ocho por ciento de los injertos criopreservados no fueron infundidos. No se observaron diferencias en la sobrevida entre los pacientes que utilizaron SPM como fuente de injerto en relación con la MO. Conclusión: Los tipos de injerto y fuentes de trasplantes no influyeron en la supervivencia de los pacientes en ambos períodos. La criopreservación se presentó como una herramienta importante para superar los desafíos logísticos relacionados con la pandemia de COVID-19, sin embargo, un porcentaje relevante de injertos criopreservados no fue utilizado. Por lo tanto, es necesario que los centros de trasplantes vuelvan a realizar TCPH con productos frescos, reduciendo el porcentaje de injertos que quedan inutilizables.
Palabras clave: COVID-19; Trasplante de Médula Ósea; Criopreservación; Supervivencia.
INTRODUÇÃO
A covid-19, inicialmente identificada na China em dezembro de 2019¹, é uma doença infecciosa altamente transmissível que se espalhou rapidamente pelo mundo. Em 3 de fevereiro de 2020, o Ministério da Saúde do Brasil decretou Emergência de Saúde Pública de Importância Nacional (Espin), em decorrência da infecção humana pelo vírus SARS-CoV-2².
O Brasil foi o primeiro país a registrar um caso da doença na América do Sul, em 26 de fevereiro de 2020³. E no dia 11 de março de 2020, a Organização Mundial da Saúde (OMS) caracterizou a covid-19 como uma pandemia em razão do surto em todos os continentes⁴.
Desde então, foram notificados 38 milhões de casos e mais de 700 mil mortes até 10 de maio de 2024, colocando o Brasil como o país com o segundo maior número de casos e óbitos no mundo⁵, emergindo como um novo epicentro da pandemia de covid-19. Tal contexto exigiu que os profissionais de saúde dedicados ao tratamento do câncer redesenhassem os cuidados oncológicos para mitigar os potenciais efeitos da infecção por covid-19 em pacientes em tratamento⁶.
Ao se realizar um transplante de células progenitoras hematopoiéticas (TCPH) alogênico não relacionado é necessário que haja uma estreita comunicação entre o centro coletor e o centro transplantador, já que esse tipo de transplante se torna mais complexo por conta da logística de transporte das células progenitoras hematopoiéticas (CPH) colhidas e enviadas ao centro transplantador⁷.
Em condições normais, a maioria dos enxertos de CPH alogênicas coletadas de doadores relacionados ou não relacionados é infundida a fresco, enquanto a criopreservação é restrita a excepcionais condições relacionadas à indisponibilidade do doador⁸. Para que o TCPH seja realizado sem riscos durante a pandemia, o Ministério da Saúde orientou os centros de transplante brasileiros a iniciar o regime de condicionamento em receptores somente após os produtos de doadores relacionados ou não relacionados terem sido entregues e criopreservados⁹. Isso permite um período adicional de monitoramento do doador em caso de exposição à covid-19 antes da infusão do enxerto¹⁰.
Em função disso, é esperado um aumento de criopreservação de CPH, uma vez que essa medida minimiza o risco de coletar um produto celular de um doador positivo para SARS-CoV-2, bem como os desafios logísticos (fechamento de fronteiras) impostos pela pandemia, a fim de garantir que os pacientes tenham um enxerto disponível no dia do transplante, o que pode impactar diretamente na sobrevida dos pacientes transplantados.
Assim, o presente estudo tem como objetivo analisar a sobrevida dos pacientes pós-TCPH imediato (até 100 dias pós-TCPH) segundo a exposição aos diferentes tipos de transplantes e fontes de enxerto, realizados na pré-pandemia e na pandemia de covid-19.
MÉTODO
Estudo de coorte retrospectivo de base hospitalar com pacientes que realizaram transplante alogênico em hospital de referência no tratamento em TCPH no município do Rio de Janeiro no período de janeiro de 2016 a dezembro de 2021. A escolha da instituição se deu em virtude do TCPH alogênico ser um procedimento de alta complexidade realizado por poucos hospitais no Estado do Rio de Janeiro. O hospital atende a pacientes adultos e crianças do RJ e demais Regiões do Brasil no âmbito do Sistema Único de Saúde (SUS).
No período estudado, foram coletados 287 enxertos. Destes, foram excluídos 31 por não apresentarem informações completas para o cálculo de sobrevida e dez por não terem sido efetivamente infundidos. Um total de 246 enxertos foi incluído no presente estudo.
Os pacientes foram divididos em dois grupos, de acordo com o período em que se realizou o transplante: grupo pré-pandemia (n = 147), de janeiro de 2016 a fevereiro de 2020, em que o TCPH e a fase de pós-transplante ocorreram no período pré-pandêmico; grupo pandêmico (n = 99), de março de 2020, mês em que foi decretado estado de pandemia de covid-19 no Brasil¹¹, até dezembro de 2021.
Os dados utilizados foram extraídos da base de dados do Centro de Transplante de Medula Óssea (Cemo) do Instituto Nacional de Câncer (INCA) por meio do Sistema de Gestão do Cemo (SGC), ferramenta de gestão do banco de dados informatizado desenvolvido pelo próprio hospital.
As seguintes variáveis foram analisadas de acordo com o receptor, doador e enxerto utilizado no TCPH. Considera-se receptor o paciente que necessita de TCPH; doador, o indivíduo cujo corpo é a fonte de obtenção das CPH; e enxerto, o produto a ser infundido no paciente.
As variáveis dos doadores incluíram o tipo de doação (relacionados ou não relacionados). Quanto ao receptor, foram analisadas faixa etária (menor de 20 anos, 20 a 59 anos e 60 anos ou mais), diagnóstico principal que levou ao transplante, data de realização do TCPH, tempo (dias) entre TCPH e óbito ou fim do acompanhamento (data da censura), sexo (masculino/feminino), tipo de doador de CPH (relacionado/não relacionado), óbito (sim/não). As variáveis do enxerto foram país de origem do enxerto, fonte de CPH (medula óssea (MO)/sangue periférico mobilizado (SPM)), criopreservação (sim/não), condição no enxerto na infusão (a fresco/criopreservada).
No método utilizado na unidade hospitalar do estudo, a criopreservação é preparada adicionando dimetilsulfóxido (DMSO - 99,9%), hidroxietilamido (16,6%) e albumina (20%) no produto de CPH, com concentrações finais de, respectivamente, 5%, 6% e 2%. Posteriormente, o produto é transferido para uma bolsa de criopreservação (100 mL) e resfriado em um freezer a -80°C.
O número de produtos de terapia celular alogênicos processados foi estimado segundo os anos avaliados (2016-2020). Foram calculadas as frequências de enxertos de acordo com a fonte, tipo de processamento e país de origem segundo o período de pré-pandemia e o período pandêmico. As frequências absolutas e relativas também foram estimadas para descrever as características sociodemográficas, o diagnóstico principal e o tipo de doador de CPH dos pacientes transplantados segundo o período de pré-pandemia e o período pandêmico. A distribuição dos óbitos foi estimada segundo o sexo, diagnóstico principal, tipo de doador de CPH e a fonte do enxerto. As diferenças nas distribuições das variáveis analisadas foram avaliadas utilizando o teste do qui-quadrado (X²) de Pearson. A sobrevida foi estimada a partir da data do transplante alogênico de CPH até a morte por qualquer causa. Os pacientes sobreviventes foram censurados na data do seu último acompanhamento, dentro de cada grupo, em até 100 dias após o transplante.
Para comparação das sobrevidas entre pré-pandemia versus pandemia, infusão a fresco versus criopreservado e uso de medula óssea versus sangue periférico mobilizado, foi utilizado o método estatístico de log-rank. Em seguida, o método de Kaplan-Meier foi usado para estimar as probabilidades de sobrevida de 100 dias pós-transplante.
Todas as análises foram realizadas com o software Stata12 (versão 17.0). Um valor-p inferior a 0,05 será considerado significativo.
O estudo foi aprovado pelos Comitês de Ética em Pesquisa (CEP) do Instituto de Estudos e Saúde Coletiva da Universidade Federal do Rio de Janeiro (Iesc/UFRJ), sob o número de parecer 6609979 (CAAE: 54261921.0.0000.5286), e do INCA sob o número de parecer 5367767 (CAAE: 54261921.0.3001.5274), de acordo com a Resolução n.º 466/1213 do Conselho Nacional de Saúde.
RESULTADOS
O número de produtos de terapia celular alogênicos processados nos últimos anos do período pré-pandemia é menor ao encontrado no período pandêmico (Gráfico 1).
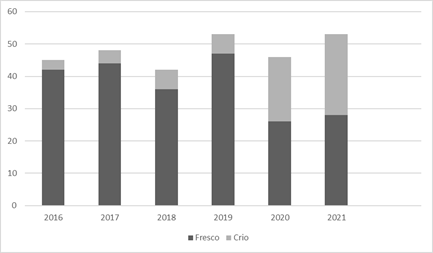
Gráfico 1. Número de produtos de terapia celular alogênicos processados por ano, de 2016 a 2021, em um hospital de referência em TCPH no município do Rio de Janeiro (n = 287)
Nota: Pré-pandemia: jan/2016 a fev/2020; pandemia: mar/2020 a dez/2021.
Quanto à origem da coleta não relacionada do produto de CPH recebido para pacientes em tratamento, foi observado que 64,7% das coletas no período pré-pandemia foram realizadas no Brasil. Já no período pandêmico, o percentual aumentou para 69,2%.
No período pré-pandêmico, somente produtos autólogos eram rotineiramente criopreservados e a maioria dos produtos alogênicos era infundida a fresco (92,5%), o que diminuiu para 54,5% no período pandêmico (Tabela 1).
Uma vez que o Brasil estava no epicentro da pandemia de covid‐19 no momento do estudo, houve a necessidade de realizar alterações na rotina de processamento e criopreservação para proteger a saúde e a segurança de nossos doadores, receptores e equipe. Por consequência, no período pandêmico, os produtos alogênicos (relacionados e não relacionados) passaram a ser criopreservados (Tabela 1).
O tipo de CPH mais utilizado no transplante em todo o período analisado foi MO (72,8%). Porém, no período pandêmico, 50,5% das coletas alogênicas foram realizadas por meio de SPM, em comparação a 11,6% antes da pandemia. Também se verificou aumento proporcional do número de criopreservações desse tipo de produto. Entre mar/2020 e dez/2021, 45 dos 99 produtos de CPH coletados, MO ou SPM, (45,5%) foram criopreservados. No período pré-pandemia, somente 7,5% dos enxertos eram criopreservados (Tabela 1).
Tabela 1. Número (n) e frequência relativa (%) segundo o processamento e a criopreservação (crio) de enxertos durante o período pré-pandemia (2016-2020)* e o período pandêmico (2020-2021)** em um hospital de referência em TCPH no município do Rio de Janeiro (n = 246)
|
|
Pré-pandemia* |
Pandemia** |
p*** |
|||
|
|
n |
% |
N |
% |
|
|
|
Sangue periférico mobilizado |
17 |
11,6 |
50 |
50,5 |
<0,0001 |
|
|
Fresco |
12 |
8,2 |
21 |
21,2 |
|
|
|
Crio |
5 |
3,4 |
29 |
29,3 |
|
|
|
Medula óssea |
130 |
88,4 |
49 |
49,5 |
<0,0001 |
|
|
Fresco |
124 |
84,3 |
33 |
33,3 |
|
|
|
Crio |
6 |
4,1 |
16 |
16,2 |
|
|
|
Total fresco |
136 |
92,5 |
54 |
54,5 |
<0,0001 |
|
|
Total crio |
11 |
7,5 |
45 |
45,5 |
|
|
|
Total |
147 |
100,0 |
99 |
100,0 |
|
|
(*) pré-pandemia: jan/2016 a fev/2020.
(**) pandemia: mar/2020 a dez/2021.
(***) teste de qui-quadrado.
Dos 246 pacientes submetidos ao TCPH alogênico no período estudado, 58,5% eram do sexo masculino, 37,4% com idade de até 19 anos, sendo esta a mais frequente em todos os períodos. Quanto às características clínicas, 35,0% apresentaram leucemia linfoide aguda (LLA) como diagnóstico principal, sendo o mais incidente tanto antes quanto durante a pandemia. O TCPH realizado com maior frequência em ambos os períodos foi o proveniente de doador relacionado (64,6%) (Tabela 2).
Tabela 2. Características sociodemográficas e diagnóstico principal dos pacientes submetidos ao transplante e número de óbitos de CPH alogênico em um hospital de referência em TCPH no município do Rio de Janeiro segundo o período pré-pandemia (2016 a 2020)* e o período pandêmico (2020 a 2021)** (n = 246)
|
Variáveis |
Pré-pandemia* |
Pandemia** |
P*** |
||
|
|
n = 147 |
% |
n = 99 |
% |
|
|
Sexo |
|
|
|
|
0,002 |
|
Masculino |
90 |
61,2 |
54 |
54,5 |
|
|
Feminino |
57 |
38,8 |
45 |
45,5 |
|
|
Faixa etária |
|
|
|
|
0,229 |
|
Até 19 anos |
60 |
41,0 |
32 |
32,1 |
|
|
20 – 39 anos |
42 |
28,7 |
30 |
30,1 |
|
|
40 – 59 anos |
38 |
26,1 |
28 |
28,2 |
|
|
60 anos ou mais |
6 |
4,2 |
9 |
9,1 |
|
|
Diagnóstico principal |
|
|
|
|
0,004 |
|
Leucemia linfoide aguda |
52 |
35,1 |
34 |
34,3 |
|
|
Leucemia mieloide aguda |
28 |
19,1 |
21 |
21,2 |
|
|
Leucemia mieloide crônica |
10 |
6,9 |
8 |
8,1 |
|
|
Linfoma não Hodgkin |
4 |
2,7 |
1 |
1,0 |
|
|
Doença de Hodgkin |
9 |
6,4 |
14 |
14,1 |
|
|
Síndrome mielodisplásica |
5 |
3,7 |
3 |
3,0 |
|
|
Outros |
38 |
26,1 |
18 |
18,2 |
|
|
Doador para TCPH |
|
|
|
|
0,404 |
|
Relacionado |
84 |
56,9 |
75 |
75,8 |
|
|
Não relacionado |
63 |
43,1 |
24 |
24,2 |
|
|
Óbitos |
13 |
8,8 |
10 |
10,1 |
|
(*) pré-pandemia: jan/2016 a fev/2020.
(**) pandemia: mar/2020 a dez/2021.
(***) teste de qui-quadrado.
TCPH = transplante de células progenitoras hematopoiéticas.
No período pré-pandemia, 13 pacientes foram a óbito. Destes, 76,9% eram do sexo masculino, 38,5% tinham entre 40 e 59 anos, 69,2% apresentavam diagnóstico de LLA, 69,2% utilizaram MO como fonte de CPH, 76,9% receberam o produto a fresco e 61,5% receberam produto de doador não relacionado. No período pandêmico, dez pacientes foram a óbito, que ocorreram com maior frequência em pacientes do sexo masculino (70%), na faixa etária de 20 a 39 anos (50%), que apresentavam diagnóstico de LLA (50%), utilizaram SPM como fonte de CPH (60%), receberam o produto a fresco (70%) e entre os que receberam CPH de doadores relacionados (80%) (Tabela 3).
Tabela 3. Caracterização dos óbitos dos pacientes submetidos a TCPH alogênicos em um hospital de referência em TCPH no município do Rio de Janeiro segundo o período de pré-pandemia (2016 a 2020)* e o período pandêmico (2020 a 2021)** (n = 23)
|
Variáveis |
Pré-pandemia* |
Pandemia** |
p*** |
||
|
|
n = 13 |
% |
n = 10 |
% |
|
|
Sexo |
|||||
|
Masculino |
10 |
76,9 |
7 |
70,0 |
0,5839 |
|
Feminino |
3 |
23,1 |
3 |
30,0 |
|
|
Faixa etária |
|
|
|
||
|
Até 19 anos |
2 |
15,4 |
2 |
20,0 |
0,4045 |
|
20 – 39 anos |
4 |
30,8 |
5 |
50,0 |
|
|
40 – 59 anos |
5 |
38,5 |
1 |
10,0 |
|
|
60 anos ou mais |
2 |
15,4 |
2 |
20,0 |
|
|
Diagnóstico Principal |
|
|
|
||
|
Leucemia linfoide aguda |
9 |
69,2 |
5 |
50,0 |
0,2733 |
|
Leucemia mieloide aguda |
1 |
7,7 |
4 |
40,0 |
|
|
Leucemia mieloide crônica |
2 |
15,4 |
0 |
0,0 |
|
|
Linfoma não Hodgkin |
0 |
0,0 |
0 |
0,0 |
|
|
Doença de Hodgkin |
1 |
7,7 |
0 |
0,0 |
|
|
Síndrome mielodisplásica |
0 |
0,0 |
0 |
0,0 |
|
|
Outros |
0 |
0,0 |
1 |
10,0 |
|
|
Tipo de Enxerto |
|
|
|
|
0,3744 |
|
Medula óssea |
9 |
69,2 |
4 |
40,0 |
|
|
Sangue periférico mobilizado |
4 |
30,8 |
6 |
60,0 |
|
|
Condição do enxerto na infusão |
|
|
0,5839 |
||
|
Fresco |
10 |
76,9 |
7 |
70,0 |
|
|
Criopreservado |
3 |
23,1 |
3 |
30,0 |
|
|
Doador para TCPH |
|
|
0,0003 |
||
|
Relacionado |
8 |
61,5 |
8 |
80,0 |
|
|
Não relacionado |
5 |
38,5 |
2 |
20,0 |
|
(*) pré-pandemia: jan/2016 a fev/2020.
(**) pandemia: mar/2020 a dez/2021.
(***) teste de qui-quadrado.
TCPH = transplante de células progenitoras hematopoiéticas.
O Gráfico 2 apresenta as curvas de sobrevida dos transplantados. Ao determinar a curva de sobrevida por condição do enxerto na infusão, foi possível observar que a curva relacionada ao enxerto criopreservado foi inferior à do enxerto a fresco na pré-pandemia. Não foi observada diferença na curva de sobrevida se comparados o tipo de doador e o tipo de enxerto durante os 100 primeiros dias pós-transplante.
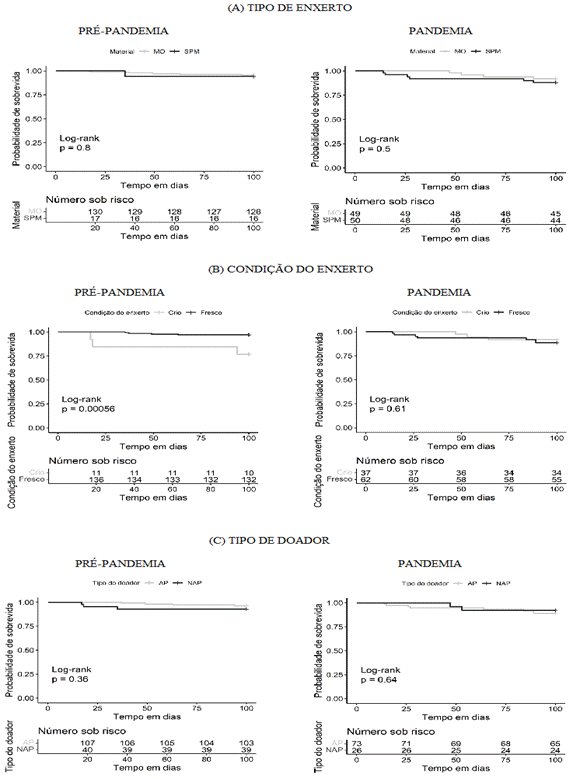
Gráfico 2. Curvas de sobrevida de 100 dias pós-TCPH em um hospital de referência em TCPH no município do Rio de Janeiro, nos períodos pré-pandemia* (n = 147) e pandemia** (n = 99) de covid-19, segundo tipo de enxerto (A), condição do enxerto na infusão (B) e tipo de doador (C)
(*) pré-pandemia: jan/2016 a fev/2020.
(**) pandemia: mar/2020 a dez/2021.
MO = medula óssea; SPM = sangue periférico mobilizado; AP = aparentado/relacionado; NAP = não aparentado/não relacionado.
DISCUSSÃO
No presente estudo, as taxas de mortalidade pós-TCPH imediato foram ligeiramente maiores no período pandêmico (10,1%) quando comparado ao período pré-pandemia (8,8%), com valor acima dos observados na literatura. O estudo de Kong et al.14 indica que a taxa de incidência cumulativa de mortalidade relacionada ao TCPH em 100 dias foi de 8,3%. A sobrevida de pacientes submetidos a TCPH tem aumentado principalmente por conta das melhorias nos cuidados de suporte, na seleção de pacientes e doadores, além das técnicas de transplante utilizadas15,16. Os 100 dias pós-transplante é um período crítico da recuperação no qual os pacientes enfrentam maior vulnerabilidade a infecções e outras complicações agudas em razão da progressiva leucopenia, tornando o paciente exposto a infecções bacterianas, fúngicas, virais e parasitárias17.
Os tipos de enxerto não influenciaram a sobrevida dos pacientes quando comparados os períodos de pré-pandemia e pandêmico. Em contraste, um estudo de Hsu et al.18, que examinou 7.379 pacientes submetidos a transplante entre 2013 e 2018, demonstrou que enxertos de SPM não relacionados criopreservados apresentaram recuperação hematopoiética retardada, aumento da recidiva e diminuição da sobrevida. Além disso, enxertos de SPM criopreservados de doadores relacionados apresentaram recuperação plaquetária retardada, sobrevida global (SG) inferior e doença de enxerto contra o hospedeiro (DECH) aguda com taxa mais elevada18.
Ao determinar a sobrevida por condição do enxerto na infusão, não foi possível observar diferenças significativas quanto à curva de sobrevida referente à criopreservação e à curva a fresco, na pré-pandemia e na pandemia. Estudos comparando CPH de SPM criopreservados versus frescos de doador alogênico mostraram resultados clínicos semelhantes em termos de SG, mortalidade sem recidiva, DECH aguda e crônica e recuperação hematopoiética19,20. Porém, Lioznov et al.21 evidenciaram taxas aumentadas de falha do enxerto nas infusões realizadas com SPM criopreservados. Em um estudo recente, Bankova et al.22 observaram que enxertos alogênicos criopreservados foram associados a enxerto tardio, taxas mais altas de falha primária do enxerto, pior SG e sobrevida livre de recidiva.
A pandemia de covid-19 mudou a conduta da terapia celular no país, entre elas a coleta e o processamento de CPH, no intuito de minimizar o risco aos doadores e receptores. Como resultado das orientações do Ministério da Saúde⁹, dado o potencial risco de exposição à covid-19 e a restrição de viagens no período, a escolha por infusão de MO a fresco reduziu de 84,3% no período pré-pandêmico para 33,3% na pandemia; por outro lado, a opção por SPM criopreservado aumentou de 3,4% para 29,3%. De acordo com o National Marrow Donor Program (NMDP), nos Estados Unidos, a opção por MO a fresco reduziu 69,9% e, inversamente, a escolha de SPM criopreservado obteve um aumento expressivo, correspondendo a 811,0%23.
Foi observada uma mudança de predileção quanto à fonte de enxerto. Antes da pandemia, a MO representava 88,4% dos enxertos processados, enquanto, no período pandêmico, esse percentual representou 49,5%. Isso foi observado em outros estudos que atribuíram essa diminuição a desafios logísticos durante a pandemia23-25. Tal fato também pode ter relação com a necessidade de submeter o doador a procedimento invasivo sob efeito de anestésicos em centro cirúrgico. Essa modalidade tem sido substituída pelo SPM, uma vez que a coleta é conduzida por procedimento pouco invasivo, com o uso de cateter periférico26.
Na pandemia, foram processados 99 produtos e infundidos 91 até 31/12/2021. Como observado, um total de oito enxertos criopreservados não foram infundidos, o que significa que 8% das doações permaneceram armazenadas. Resultado semelhante ao estudo de Allan27, realizado no Canadá, em que aproximadamente 7% dos enxertos criopreservados nunca foram infundidos. Um estudo realizado pelo registro de doadores da Alemanha concluiu que 5-10% dos produtos criopreservados não serão eventualmente transfundidos28. Isso gera preocupações éticas para os doadores que podem ter sofrido não apenas inconvenientes ligados à coleta de CPH, mas também exposição potencial ao SARS-CoV-2 como resultado do atendimento em centros de coleta em áreas com alta prevalência da doença29. É importante ressaltar que a infusão de células frescas pode reduzir os custos associados ao processamento, criopreservação e armazenamento⁸.
O número de produtos de terapia celular alogênicos processados tem permanecido relativamente constante. Resultado semelhante ao encontrado no por Valentini et al.24 e Tanhehco, Schwartz30.
O estudo também caracterizou os pacientes quanto ao sexo e à idade, e encontrou os percentuais próximos entre os três grupos, sendo a maioria do sexo masculino e uma idade média de 33 anos, semelhante aos resultados de pesquisas realizadas em Minas Gerais e no Rio grande do Norte31,32. Estudo desenvolvido em centros nos EUA e no Canadá, entre 2006 e 2012, também apresentou um maior número de homens (63%)33. Assim, ao considerar os estudos analisados, percebe-se um predomínio de pacientes adultos, do sexo masculino, que foram submetidos a TCPH alogênico, convergindo com os resultados deste estudo.
Quanto ao diagnóstico que mais levou ao transplante alogênico, a LLA prevaleceu em ambos os períodos (35,1% e 34,34%, respectivamente), o que estabelece relação direta com a faixa de idade dos pacientes analisados, já que a faixa etária com maior percentual foi de até 19 anos nos períodos analisados (41,0% e 32,1%, respectivamente). É o tipo de leucemia mais prevalente em crianças, com maior incidência entre 2 e 5 anos, sendo responsável por 80% dos casos infantis e 20% em adultos34, e é quatro vezes mais frequente do que a leucemia mieloide aguda (LMA)35, a segunda doença mais frequente neste estudo. A LLA também foi a principal doença que levou à óbito (69,2% e 50,0%, respectivamente).
Para muitos autores, a criopreservação de CPH pode ser considerada uma opção na pandemia de covid-19, equilibrando os riscos e os benefícios do procedimento36,37. As desvantagens desse procedimento estão relacionadas à potencial toxicidade ligada ao criopreservante DMSO, à perda da viabilidade celular e a custos adicionais38.
Uma limitação deste estudo é que, além da heterogeneidade da coorte, que recebeu uma variedade de regimes de condicionamento e profilaxia de DECH, não houve uma diferenciação entre os transplantes quanto à compatibilidade do antígeno leucocitário humano (HLA). No entanto, este artigo fornece uma visão sobre como um hospital de referência em TCPH no Brasil foi afetado e continuou a funcionar de forma eficiente durante a pandemia de covid-19.
CONCLUSÃO
O estudo apresenta evidências científicas relevantes quanto ao perfil epidemiológico, clínico e à sobrevida de pacientes submetidos a TCPH alogênico, considerando um contexto de crise global que foi a pandemia de covid-19. A criopreservação de CPH alogênica é uma ferramenta importante em um momento em que houve muita incerteza em termos de disponibilidade e transporte de enxertos, pois garantiu que os pacientes condicionados realizassem o TCPH com segurança. Contudo, o significativo número de produtos de CPH não transfundidos é problemático e requer uma atenção individualizada da melhor abordagem para cada paciente.
Porém, este estudo indica que é preciso cautela na utilização de produtos criopreservados para transplante alogênico, embora não tenha havido diferença significativa na sobrevida entre os pacientes que utilizaram produtos frescos em comparação com criopreservados. Um acompanhamento mais longo e uma investigação mais aprofundada dessas descobertas são necessários para explorar completamente como a criopreservação e a idade dos enxertos alogênicos podem impactar a segurança e a eficácia do transplante.
Além disso, é necessária uma investigação detalhada que considere os diversos fatores que podem ter contribuído para o aumento das mortes durante a pandemia. A análise deve incluir aspectos como o impacto da covid-19 nas condições de saúde dos pacientes, o acesso aos cuidados médicos, e as possíveis complicações decorrentes tanto do vírus quanto das medidas de isolamento social.
É importante que os centros de transplante e os registros de doadores não relacionados incentivem a prática de TCPH a fresco, no intuito de protegerem os interesses dos doadores, pacientes e na minimização de custos para a instituição.
AGRADECIMENTOS
A Luciglei Nazareth Baiense e a Adriano Bayão Rocha da Silva pelo apoio dado na condução da coleta de dados.
CONTRIBUIÇÕES
Pedro Felipe Couto Vieira contribuiu na concepção e no delineamento do estudo; na análise e interpretação dos dados; na redação. Jackeline Christiane Pinto Lobato Vasconcelos e Amanda de Moura Souza contribuíram na concepção e no delineamento do estudo; na análise e interpretação dos dados; na redação e revisão crítica. Carla Cristina Pedrosa de Lira contribuiu na concepção e no delineamento do estudo; na redação e revisão crítica. Rômulo Gonçalves Galvani e Marina Vieira Agostinho Pereira contribuíram na análise e interpretação dos dados; na redação e revisão crítica. Todos os autores aprovaram a versão final do manuscrito a ser publicada.
DECLARAÇÃO DE CONFLITO DE INTERESSES
Nada a declarar.
FONTES DE FINANCIAMENTO
Não há.
REFERÊNCIAS
1. Phelan AL, Katz R, Gostin LO. The novel coronavirus originating in Wuhan, China: challenges for global health governance. JAMA. 2020;323(8):709-10. doi: https://doi.org/10.1001/jama.2020.1097
2. Ministério da Saúde (BR). Secretaria de Atenção Especializada à Saúde (SAES). Nota Técnica Nº 25/2020-CGSNT/DAET/SAES/MS. Brasília, DF: MS; 2020 [internet]. [acesso 2023 jul 8]. Disponível em: https://www.gov.br/saude/pt-br/assuntos/covid-19/notas-tecnicas/2020/nota-tecnica-no-25-2020-cgsnt-daet-saes-ms/view
3. Nações Unidas. Latin America and the Caribbean and the COVID-19 pandemic economic and social effects. Esp Report Covid-19 [Internet]. 2020 [acesso 2023 jul 3];1:1-14. Disponível em: https://repositorio.cepal.org/bitstream/handle/11362/45351/1/S2000263_en.pdf
4. World Health Organization [Internet]. Geneva: WHO; 2020. WHO Director-General's opening remarks at the media briefing on COVID-19 - 11 March 2020, 2020 mar 11. [acesso 2024 fev 3]. Disponível em: https://www.who.int/director-general/speeches/detail/who-director-general-s-opening-remarks-at-the-media-briefing-on-covid-19---11-march-2020
5. Painel Coronavírus [Internet]. Brasília, DF: MS; 2023. [acesso 2024 maio 18]. Disponível em: https://Covid.saude.gov.br/
6. The Lancet Oncology. COVID-19: global consequences for oncology [Editorial]. Lancet Oncol. 2020;21(4):467. doi: https://doi.org/10.1016/s1470-2045(20)30175-3
7. Sahu KK, Lal A, Mishra AK. Latest updates on COVID-2019: a changing paradigm shift. J Med Virol. 2020;92(6):533-5. doi: https://doi.org/10.1002%2Fjmv.25760
8. Frey NV, Lazarus HM, Goldstein SC. Has allogeneic stem cell cryopreservation been given the 'cold shoulder'? An analysis of the pros and cons of using frozen versus fresh stem cell products in allogeneic stem cell transplantation. Bone Marrow Transplant. 2006;38(6):399-405. doi: https://doi.org/10.1038/sj.bmt.1705462
9. Ministério da Saúde (BR). Secretaria de Atenção Especializada à Saúde (SAES). Nota Técnica nº 36/2020-CGSNT/DAET/SAES/MS. Brasília, DF: MS; 2020. [acesso: 2023 maio 18]. Disponível em: https://www.gov.br/saude/pt-br/coronavirus/publicacoes-tecnicas/notas-tecnicas/nota-tecnica-no-36-2020-cgsnt-daet-saes-ms/view
10. Jaiswal SR, Zaman S, Chakrabarti A, et al. Improved outcome of refractory/relapsed acute myeloid leukemia after post-transplantation cyclophosphamide-based haploidentical transplantation with myeloablative conditioning and early prophylactic granulocyte colony-stimulating factor-mobilized donor lymphocyte infusions. Biol Blood Marrow Transplant. 2016;22(10):1867-73. doi: https://doi.org/10.1016/j.bbmt.2016.07.016
11. Ministério da Saúde (BR) [Internet]. Brasília, DF: Ministério da Saúde; 2020. Ministério da Saúde declara transmissão comunitária nacional, 2020 mar 21. [acesso 2023 maio 18; atualizado 2022 nov 1]. Disponível em: https://www.gov.br/saude/pt-br/assuntos/noticias/2020/marco/ministerio-da-saude-declara-transmissao-comunitaria-nacional#:~:text=O%20Minist%C3%A9rio%20da%20Sa%C3%BAde%20declarou,se%20unir%20contra%20o%20v%C3%ADrus
12. StataR [Internet]. Versão 17.0. Lakeway: StataCorp LLC; 1996–2024c. [acesso 2023 nov 20]. Disponível em: https://www.stata.com/
13. Conselho Nacional de Saúde (BR). Resolução n° 466, de 12 de dezembro de 2012. Aprova as diretrizes e normas regulamentadoras de pesquisas envolvendo seres humanos. Diário Oficial da União, Brasília, DF. 2013 jun 13; Seção I:59.
14. Kong SG, Jeong S, Lee S, et al. Early transplantation-related mortality after allogeneic hematopoietic cell transplantation in patients with acute leukemia. BMC Cancer. 2021;21(1):177. doi: https://doi.org/10.1186/s12885-021-07897-3
15. Hahn T, McCarthy PL Jr, Hassebroek A, et al. Significant improvement in survival after allogeneic hematopoietic cell transplantation during a period of significantly increased use, older recipient age, and use of unrelated donors. J Clin Oncol. 2013;31(19):2437-49. Errata: J Clin Oncol. 2013;31(23):2977 doi: https://doi.org/10.1200/jco.2012.46.6193
16. McDonald GB, Sandmaier BM, Mielcarek M, et al. Survival, nonrelapse mortality, and relapse-related mortality after allogeneic hematopoietic cell transplantation: comparing 2003-2007 versus 2013-2017 cohorts. Ann Intern Med. 2020;172(4):229-39. doi: https://doi.org/10.7326%2FM19-2936
17. Marques A, Proença S, Machado C, et al. Qualidade de vida nos primeiros seis meses pós-transplante de células-tronco hematopoéticas. Texto Contexto Enferm. 2017;26(3):e5040016. doi: https://doi.org/10.1590/0104-07072017005040016
18. Hsu JW, Farhadfar N, Murthy H, et al. The effect of donor graft cryopreservation on allogeneic hematopoietic cell transplantation outcomes: a center for international blood and marrow transplant research analysis. implications during the covid-19 pandemic. Transplant Cell Ther. 2021;27(6):507-16. doi: https://doi.org/10.1016/j.jtct.2021.03.015
19. Kim DH, Jamal N, Saragosa R, et al. Similar outcomes of cryopreserved allogeneic peripheral stem cell transplants (PBSCT) compared to fresh allografts. Biol Blood Marrow Transplant. 2007;13(10):1233-43. doi: https://doi.org/10.1016/j.bbmt.2007.07.003
20. Alotaibi AS, Prem S, Chen S, et al. Fresh vs. frozen allogeneic peripheral blood stem cell grafts: A successful timely option. Am J Hematol. 2021;96(2):179-87. Erratum in: Am J Hematol. 2021;96(10):1345. doi: https://doi.org/10.1002/ajh.26033
21. Lioznov M, Dellbrügger C, Sputtek A, et al. Transportation and cryopreservation may impair haematopoietic stem cell function and engraftment of allogeneic PBSCs, but not BM. Bone Marrow Transplant. 2008;42(2):121-8. doi: https://doi.org/10.1038/bmt.2008.93
22. Bankova AK, Caveney J, Yao B, et al. Real-World Experience of Cryopreserved Allogeneic Hematopoietic Grafts during the COVID-19 Pandemic: a single-center report. Transplant Cell Ther. 2022;28(4):215.e1-215.e10. doi: https://doi.org/10.1016/j.jtct.2022.01.010
23. Auletta JJ, Novakovich JL, Stritesky GL, et al. Meeting the demand for unrelated donors in the midst of the COVID-19 pandemic: rapid adaptations by the national marrow donor program and its network partners ensured a safe supply of donor products. Transplant Cell Ther. 2021;27(2):133-41. doi: https://doi.org/10.1016/j.jtct.2020.10.014
24. Valentini CG, Chiusolo P, Bianchi M, et al. Coronavirus disease 2019 pandemic and allogeneic hematopoietic stem cell transplantation: a single center reappraisal. Cytotherapy. 2021;23(7):635-40. doi: https://doi.org/10.1016/j.jcyt.2020.12.001
25. Jöris MM, Schmidt AH, Bernas SN, et al. Impact of COVID-19 pandemic on global unrelated stem cell donations in 2020-Report from World Marrow Donor Association. Bone Marrow Transplant. 2022;57(6):1021-4. doi: https://doi.org/10.1038/s41409-022-01667-w
26. Fabricius WA, Ramanathan M. Review on haploidentical hematopoietic cell transplantation in patients with hematologic malignancies. Adv Hematol. 2016;2016:5726132. doi: https://doi.org/10.1155/2016/5726132
27. Allan DS. A Timely CIBMTR analysis of how cryopreservation impacts allogeneic hematopoietic cell transplantation to apply in the COVID Era. Transplant Cell Ther. 2021;27(6):446-7. doi: https://doi.org/10.1016/j.jtct.2021.05.009
28. Schmidt AH, Buk D, Platz A, et al. Cryopreservation for all is no option in unrelated stem cell transplantation. comment on dholaria b, et al. securing the graft during pandemic: are we ready for cryopreservation for all? Biol Blood Marrow Transplant. 2020;26(11):e298-9. doi: https://doi.org/10.1016/j.bbmt.2020.08.011
29. Purtill D, Hutchins C, Kennedy G, et al. Good engraftment but quality and donor concerns for cryopreserved hemopoietic progenitor cell products collected during the COVID-19 pandemic. Transplant Cell Ther. 2021;27(12):1022.e1-1022.e6. doi: https://doi.org/10.1016/j.jtct.2021.09.012
30. Tanhehco YC, Schwartz J. How the COVID-19 pandemic changed cellular therapy at Columbia University Irving Medical Center/NewYork-Presbyterian Hospital. Transfusion. 2020;60(9):1905-9. doi: https://doi.org/10.1111/trf.15956
31. Abreu MHNG, Oliveira IR, Resende RG, et al. Análise socieodemográfica e clínica de pacientes submetidos ao transplante alogênico de células-troncos hematopoiéticas. Pesq Bras Odontoped Clin Integr. 2012;12(3):345-50. doi: https://doi.org/10.4034/PBOCI.2012.123.07
32. Campos de Azevedo I, Ferreira Júnior MA, Pereira de Aquino LA, et al. Epidemiologic profile of patients transplanted with hematopoietic stem cells in a reference service in the state of Rio Grande do Norte, Brazil. Transplant Proc. 2018;50(3):819-23. doi: https://doi.org/10.1016/j.transproceed.2018.02.015
33. Wagner Junior JE, Eapen M, Carter S, et al. Blood and marrow transplant clinical trials network. one-unit versus two-unit cord-blood transplantation for hematologic cancers. N Engl J Med. 2014;371(18):1685-94. doi: https://doi.org/10.1056/nejmoa1405584
34. Farias MG, Castro SM. Diagnóstico laboratorial das leucemias linfoides agudas. J Bras Patol Med Lab. 2004;40(2):91-8. doi: https://doi.org/10.1590/S1676-24442004000200008
35. Barbosa CM, Nakamura C, Terreri MT, et al. Manifestações músculo-esqueléticas como apresentação inicial das leucemias agudas na infância. J Pediatr (Rio J). 2002;78(6):481-4. doi: https://doi.org/10.1590/S0021-75572002000600007
36. Jacob RP, Flynn J, Devlin SM, et al. Universal engraftment after allogeneic hematopoietic cell transplantation using cryopreserved cd34-selected grafts. Transplant Cell Ther. 2021;27(8):697.e1-697.e5. doi: https://doi.org/10.1016/j.jtct.2021.04.026
37. Kanda Y, Inoue M, Uchida N, et al. Cryopreservation of unrelated hematopoietic stem cells from a blood and marrow donor bank during the COVID-19 pandemic: a nationwide survey by the japan marrow donor program. Transplant Cell Ther. 2021;27(8):664.e1-664.e6. doi: https://doi.org/10.1016/j.jtct.2021.04.022
38. Schäfer AK, Waterhouse M, Follo M, et al Phenotypical and functional analysis of donor lymphocyte infusion products after long-term cryopreservation. Transfus Apher Sci. 2020;59(1):102594. doi: https://doi.org/10.1016/j.transci.2019.06.022
Recebido em 10/6/2024
Aprovado em 7/8/2024
Editora-científica: Anke Bergmann. Orcid iD: https://orcid.org/0000-0002-1972-8777
![]()
Este é um artigo publicado em acesso aberto (Open Access) sob a licença Creative Commons Attribution, que permite uso, distribuição e reprodução em qualquer meio, sem restrições, desde que o trabalho original seja corretamente citado.