RELATO DE CASO
Tumor de Krukenberg em Longo Tempo de Remissão: Relato de Caso
Krukenberg Tumor in Long-Term Remission: Case Report
Tumor de Krukenberg en Largo Período de Remisión: Informe de Caso
https://doi.org/10.32635/2176-9745.RBC.2025v71n2.4926
Isabelle Ariane Wagner1; Tadeu Ferreira de Paiva Júnior2
1Pesquisadora autônoma. Florianópolis (SC), Brasil. E-mail: isabelle.awagner@gmail.com. Orcid iD: https://orcid.org/0000-0001-6472-7581
2Ynova Pesquisa Clínica. Florianópolis (SC), Brasil. E-mail: tadeufpaivajr@gmail.com. Orcid iD: https://orcid.org/0009-0006-7426-8095
Endereço para correspondência: Isabelle Ariane Wagner. Rua Menino Deus, 63 - Bloco A - Sala 303 – Centro. Florianópolis (SC), Brasil. CEP 88020-210. E-mail: isabelle.awagner@gmail.com
RESUMO
Introdução: O tumor de Krukenberg compreende um tumor metastático raro e agressivo que faz parte dos diagnósticos diferenciais das massas ovarianas. Origina-se principalmente do trato gastrointestinal, especialmente do estômago e cólon. Sua sobrevida mediana ao diagnóstico é de 16 meses. Relato do caso: Paciente de 35 anos, hígida, queixava-se de dor abdominal baixa e dispareunia há um ano, com ultrassonografia transvaginal evidenciando massa extensa em ovário esquerdo. Por meio da investigação, foi realizada colonoscopia revelando adenocarcinoma de retossigmoide. A avaliação posterior compreendeu a análise do painel genético cujo resultado foi negativo e a revelação de metástase no fígado, no peritônio e no ovário, este último denominado tumor de Krukenberg. Após tratamento envolvendo quimioterapia, cirurgias de retossigmoidectomia com linfadenectomia e salpingo-oforectomia bilateral, cirurgias de citorredução peritoneal e de metastasectomia hepática, as duas últimas associadas à quimioterapia intraperitoneal hipertérmica, encontra-se assintomática, com qualidade de vida e em remissão completa cinco anos após o diagnóstico. Conclusão: Relatar o caso de tumor de Krukenberg com tempo de remissão mais prolongado do que o descrito em literatura, possivelmente pelas terapias combinadas utilizadas e perfil molecular favorável.
Palavras-chave: Tumor de Krukenberg/diagnóstico; Doenças Ovarianas; Sobrevida; Metástase Neoplásica.
ABSTRACT
Introduction: Krukenberg tumor is a rare and aggressive metastatic tumor that is part of the differential diagnosis of ovarian masses. It originates mainly from the gastrointestinal tract, especially the stomach and colon. Its median survival at diagnosis is 16 months. Case report: A 35-year-old healthy patient complained of lower abdominal pain and dyspareunia for one year, with a transvaginal ultrasound showing an extensive mass in the left ovary. Through the investigation, a colonoscopy was performed revealing rectosigmoid adenocarcinoma. The subsequent evaluation included analysis of the genetic panel, the result of which was negative, and the revelation of metastases in the liver, peritoneum, and ovary, the latter called Krukenberg tumor. After treatment involving chemotherapy, rectosigmoidectomy with lymphadenectomy and bilateral salpingo-oophorectomy, peritoneal cytoreduction, and hepatic metastasectomy surgeries, the latter two associated with hyperthermic intraperitoneal chemotherapy, the patient is asymptomatic, with quality of life and in complete remission five years after diagnosis. Conclusion: Case report of Krukenberg tumor with a longer remission time than described in the literature, possibly due to the combined therapies used and favorable molecular profile.
Key words: Krukenberg Tumor/diagnosis; Ovarian Diseases; Survival; Neoplasm Metastasis.
RESUMEN
Introducción: El tumor de Krukenberg es un tumor metastásico raro y agresivo que forma parte del diagnóstico diferencial de las masas ováricas. Se origina principalmente en el tracto gastrointestinal, especialmente en el estómago y el colon. Su mediana de supervivencia al momento del diagnóstico es de 16 meses. Informe del caso: Paciente sana de 35 años, que consultó por dolor abdominal bajo y dispareunia de un año de evolución, con ecografía transvaginal que mostró masa extensa en ovario izquierdo. A través de la investigación, se realizó una colonoscopia que reveló un adenocarcinoma rectosigmoideo. La evaluación posterior incluyó el análisis del panel genético, cuyo resultado fue negativo y la revelación de metástasis en hígado, peritoneo y ovario, este último denominado tumor de Krukenberg. Luego de un tratamiento que incluyó quimioterapia, cirugías de rectosigmoidectomía con linfadenectomía y salpingooforectomía bilateral, cirugía de citorreducción peritoneal y metastasectomía hepática, estas dos últimas asociadas a quimioterapia intraperitoneal hipertérmica, la paciente se encuentra asintomática, con calidad de vida y en remisión completa a cinco años del diagnóstico. Conclusión: Se reporta un caso de tumor de Krukenberg con tiempo de remisión mayor al descrito en la literatura, posiblemente debido a las terapias combinadas utilizadas y al perfil molecular favorable.
Palabras clave: Tumor de Krukenberg/diagnóstico; Enfermedades del Ovario; Sobrevida; Metástasis de la Neoplasia.
INTRODUÇÃO
O tumor de Krukenberg é uma forma rara de tumor metastático que afeta os ovários, originando-se comumente do trato gastrointestinal, especialmente do estômago e cólon¹. Embora o estômago ainda seja o órgão mais prevalente como sítio primário (76%)²,³, o cólon tem se mostrado cada vez mais relevante⁴ em razão do aumento da incidência do câncer colorretal. Caracteriza-se histologicamente por células em anel de sinete produtoras de mucina⁵, sendo um importante diagnóstico diferencial de massas ovarianas⁶.
Acredita-se que a downregulation de E-caderina no sítio primário contribui para a metástase ao ovário⁷. Existem quatro vias de propagação: continuidade, contiguidade, hematogênica ou linfática⁸, dependendo do sítio primário⁶. Tumores gástricos tendem à via linfática, enquanto adenocarcinomas de cólon propagam-se por via hematogênica por sua intensa vascularização intestinal⁸.
A idade mediana ao diagnóstico é 48 anos, frequentemente na perimenopausa⁹. Tumores bilaterais são comuns⁹, e a ooforectomia bilateral integra o tratamento¹⁰. A sobrevida mediana é de 16 meses⁹, mas fatores como extensão metastática e abordagem terapêutica influenciam significativamente o prognóstico⁹. A mediana se amplia para 23 meses quando a metástase é confinada ao ovário e reduz para 13,5 meses quando há metástase para outros sítios, além do ovário⁹. Não só a extensão da metástase, outros fatores relacionados à piora de sobrevida são presença de ascite e sítio primário gástrico⁹. Existem fatores que aumentam a sobrevida e estão envolvidos com o tratamento da doença: metastasectomia¹¹, ressecção cirúrgica do tumor primário¹², cirurgia citorredutora13-15 e quimioterapia intraperitoneal hipertérmica (HIPEC)¹⁵, além do tratamento com quimioterapia16.
O objetivo do presente estudo é relatar o caso de uma paciente portadora de tumor de Krukenberg há mais de cinco anos, atualmente em remissão clínica, apresentando uma sobrevida consideravelmente maior do que a mediana descrita em literatura científica. A pesquisa foi conduzida após a aprovação do Comitê de Ética em Pesquisa (CEP) do Centro de Pesquisas Oncológicas (Cepon), sob o número de parecer 6.995.879 (CAAE: 81627524.2.0000.5355), com base na Resolução n.º 466/2012¹⁷ do Conselho Nacional de Saúde.
RELATO DO CASO
Paciente do sexo feminino, 35 anos, previamente hígida, gesta dois, para um, aborto um, com histórico de abortamento espontâneo há um ano. Queixava-se de dor de forte intensidade em baixo ventre e dispareunia de profundidade. Realizada ultrassonografia transvaginal (USG-TV), em janeiro de 2019, com visualização de coleção anexial heterogênea em ovário esquerdo medindo 7,4 x 5,4 x 8,4 cm, foi levantada a hipótese de cisto de corpo lúteo pós-aborto, prescrito acetato de medroxiprogesterona, sem melhora. Uma nova USG-TV foi solicitada em três meses, evidenciando permanência da massa anexial à esquerda, com projeção ao fundo de saco posterior. Por conta da expansividade da lesão, foram realizadas endoscopia digestiva alta e colonoscopia, esta última apontando uma lesão ulcerovegetante em junção retossigmoide, cuja biópsia revelou adenocarcinoma moderadamente diferenciado, ulcerado, infiltrando a lâmina própria. No momento do diagnóstico, a paciente referia perda ponderal de 3 kg na última semana e episódios prévios de hematoquezia, antes associados com doença hemorroidária. Posteriormente, foram revelados possíveis implantes neoplásicos em tomografia computadorizada (TC) de abdome e pelve: uma lesão hipodensa no fígado, além de lesão pélvica cística (Figura 1) — caracterizada como tumor de Krukenberg. Após duas semanas do diagnóstico inicial, optou-se, em fevereiro de 2019, pela realização de retossigmoidectomia com linfadenectomia, salpingo-oforectomia bilateral, além da ressecção de um implante peritoneal em fundo de Saco de Douglas, recebendo, com as peças cirúrgicas obtidas, o estadiamento patológico pT4apN2bpM1c, com margens de ressecção cirúrgica livres de neoplasia. Foi feita a execução do perfil molecular por pirosequenciamento, resultante em KRAS e NRAS de tipo selvagem, painel de câncer hereditário com ausência de variante patogênica e pesquisa de instabilidade microssatélite negativa com um único achado de variante de significado clínico incerto (VUS) no gene BLM. Após a realização de 11 ciclos de quimioterapia adjuvante quinzenalmente entre março e agosto de 2019 com protocolo FOLFOX (ácido folínico, 5-fluorouracil e oxaliplatina) + cetuximabe, houve resposta parcial detectada pela remanescência de metástases hepáticas na ressonância magnética (RM) de abdome.
Dessa forma, em razão da resposta apresentada e considerando a ressecabilidade das metástases, após oito meses do diagnóstico e um mês após a quimioterapia adjuvante, a paciente foi submetida em setembro de 2019 à HIPEC com oxaliplatina somada a hepatectomia parcial e peritoniectomia, cujo anatomopatológico demonstrou resposta completa no peritônio. Em julho de 2020, por conta de uma recidiva de implante neoplásico em fígado, além do aparecimento de implante pré-sacral, apontados em nova PET-CT dez meses após a HIPEC, optou-se por uma cirurgia citorredutora com ressecção das metástases, além de nova HIPEC, agora com mitomicina. Subsequentemente à última cirurgia, entre outubro de 2020 e abril de 2021, a paciente teve indicação de 13 ciclos de quimioterapia com FOLFOX, seguidos por retirada da oxaliplatina e manutenção com 5-fluorouracil + ácido folínico por seis sessões. Em agosto de 2021, por TC de tórax e RM de abdome, ambos sem evidência de doença, a paciente atingiu resposta completa ao tratamento. Houve posterior modificação para quimioterapia oral com capecitabina a fim de garantir maior comodidade para a paciente. Cinco anos após o diagnóstico, encontra-se assintomática e em remissão completa há mais de três anos, sem evidência de doença.
DISCUSSÃO
Este caso destaca-se pela remissão prolongada do tumor de Krukenberg, apresentando uma mediana de sobrevida muito superior à relatada na literatura científica. Apesar da apresentação inicial desfavorável da paciente, houve uma resposta notável ao tratamento. Após cinco anos do diagnóstico, a paciente permanece há mais de três anos sem evidência de doença e com qualidade de vida preservada. Este desfecho é atribuído a fatores como o status KRAS selvagem¹⁸,¹⁹ e a abordagem terapêutica adotada¹¹-¹⁶, incluindo citorredução cirúrgica, ressecção de metástases e quimioterapia.
O relato contrasta positivamente com a mediana de sobrevida documentada na literatura, que é frequentemente limitada. Além disso, enquanto a mediana de idade ao diagnóstico é em torno de 48 anos, com alta prevalência em pacientes na perimenopausa⁹, o caso descrito envolve uma paciente de 35 anos, destacando a relevância de considerar esse diagnóstico mesmo em idades mais jovens. A presença de metástases bilaterais, típicas em até 80% dos casos¹⁰, também foi observada, reforçando a apresentação característica, embora em faixa etária atípica.
No nível molecular, o status KRAS selvagem identificado na paciente é associado a uma melhor resposta ao cetuximabe¹⁹, anticorpo monoclonal utilizado no tratamento do câncer colorretal, fator que provavelmente contribuiu para o prognóstico favorável. Em contraste, a presença de mutações nesse gene está ligada a uma sobrevida reduzida¹⁸.
As abordagens terapêuticas adotadas foram determinantes para os resultados alcançados. Há destaque para a citorredução cirúrgica como essencial para melhorar os desfechos, abordagem esta empregada neste caso em múltiplas etapas, incluindo retossigmoidectomia, salpingo-oforectomia bilateral e hepatectomias parciais. A HIPEC¹⁵, eficaz na redução da carga tumoral peritoneal, também foi utilizada com sucesso. A combinação do protocolo FOLFOX com a HIPEC ilustra a integração de terapias para otimizar os resultados, alinhando-se às recomendações mais recentes da literatura¹³.
Este relato sublinha a relevância de estratégias diagnósticas e terapêuticas avançadas para casos de tumor de Krukenberg, enfatizando a possibilidade de desfechos favoráveis mesmo em cenários complexos.
CONCLUSÃO
O tumor de Krukenberg representa um desafio clínico significativo, tanto no diagnóstico quanto no tratamento, dada a sua origem metastática e os complexos fatores que influenciam a sobrevida dos pacientes. É crucial que os profissionais de saúde estejam cientes dessa possibilidade na avaliação diferencial das massas ovarianas para garantir uma abordagem de tratamento apropriada e melhorar os prognósticos dos pacientes.
CONTRIBUIÇÕES
Ambos os autores contribuíram substancialmente na concepção e no planejamento do estudo; na obtenção, análise e interpretação dos dados; na redação e revisão crítica; e aprovaram a versão final a ser publicada.
DECLARAÇÃO DE CONFLITO DE INTERESSES
Nada a declarar.
FONTES DE FINANCIAMENTO
Não há.
REFERÊNCIAS
1. Bas Y, Kalyoncu A, Bulgan A, et al. Synchronized bilateral giant krukenberg tumor originating from the colon. Turkiye Klinikleri J Case Rep. 2018;26(1):40-4. doi: https://www.doi.org/10.5336/caserep.2017-55128
2. Ionescu O, Balescu I, Bacalbasa N. Krukenberg tumors. Prognostic factors, surgical treatment and survival benefit. A literature review. Gineco.eu. 2016;12:202-4. doi: https://www.doi.org/10.18643/gieu.2016.202
3. Yada-Hashimoto N, Yamamoto T, Kamiura S, et al. Metastatic ovarian tumors: a review of 64 cases. Gynecol Oncol. 2003;89(2):314-7. doi: https://www.doi.org/10.1016/s0090-8258(03)00075-1
4. Jiang R, Tang J, Cheng X, et al. Surgical treatment for patients with different origins of Krukenberg tumors: outcomes and prognostic factors. Eur J Surg Oncol. 2009;35(1):92-7. doi: https://www.doi.org/10.1016/j.ejso.2008.05.006
5. Novak C, Gray LA. Krukenberg tumor of the ovary: clinical and pathological study of four cases. Surg Gynecol Obstet. 1938;66:157‑65.
6. Moore RG, Chung M, Granai CO, et al. Incidence of metastasis to the ovaries from nongenital tract primary tumors. Gynecol Oncol. 2004;93(1):87-91. doi: https://www.doi.org/10.1016/j.ygyno.2003.12.039
7. Kuwabara Y, Yamada T, Yamazaki K, et al. Establishment of an ovarian metastasis model and possible involvement of E-cadherin down-regulation in the metastasis. Cancer Sci. 2008;99(10):1933-9. doi: https://www.doi.org/10.1111/j.1349-7006.2008.00946.x
8. Yamanishi Y, Koshiyama M, Ohnaka M, et al. Pathways of metastases from primary organs to the ovaries. Obstet Gynecol Int. 2011;2011:1-6. doi: https://www.doi.org/10.1155/2011/612817
9. Wu F, Zhao X, Mi B, et al. Clinical characteristics and prognostic analysis of Krukenberg tumor. Mol Clin Oncol. 2015;3(6):1323-8. doi: https://www.doi.org/10.3892/mco.2015.634
10. Zulfiqar M, Koen J, Nougaret S, et al. Krukenberg tumors: update on imaging and clinical features. AJR Am J Roentgenol. 2020;215(4):1020-9. doi: https://www.doi.org/10.2214/AJR.19.22184
11. Jiang R, Tang J, Cheng X, et al. Surgical treatment for patients with different origins of Krukenberg tumors: outcomes and prognostic factors. Eur J Surg Oncol. 2009;35(1):92-7. doi: https://www.doi.org/10.1016/j.ejso.2008.05.006
12. Jun SY, Park JK. Metachronous ovarian metastases following resection of the primary gastric cancer. J Gastric Cancer. 2011;11(1):31-7. doi: https://www.doi.org/10.5230/jgc.2011.11.1.31
13. Xu KY, Gao H, Lian ZJ, et al. Clinical analysis of Krukenberg tumours in patients with colorectal cancer-a review of 57 cases. World J Surg Oncol. 2017;15(1):25. doi: https://www.doi.org/10.1186/s12957-016-1087-y
14. McCormick CC, Giuntoli II RL , Gardner GJ, et al. The role of cytoreductive surgery for colon cancer metastatic to the ovary. Gynecol Oncol. 2007;105(3):791-5. doi: https://www.doi.org/10.1016/j.ygyno.2007.02.025
15. Lionetti R, De Luca M, Travaglino A, et al. Treatments and overall survival in patients with Krukenberg tumor. Arch Gynecol Obstet. 2019;300(1):15-23. doi: https://www.doi.org/10.1007/s00404-019-05167-z
16. Lu W, Yuan L, Liu X, et al. Identification of prognostic factors for Krukenberg tumor. Gynecol Minim Invasive Ther. 2013;2(2):52-6. doi: https://www.doi.org/10.1016/j.gmit.2013.02.006
17. Conselho Nacional de Saúde (BR). Resolução n° 466, de 12 de dezembro de 2012. Aprova as diretrizes e normas regulamentadoras de pesquisas envolvendo seres humanos. Diário Oficial da União, Brasília, DF. 2013 jun 13; Seção I:59.
18. Kemps PG, Bol M, Steller EJA, et al. Colon carcinoma presenting as ovarian metastasis. Radiol Case Rep. 2021;16(9):2799-803. doi: https://www.doi.org/10.1016/j.radcr.2021.06.072
19. Formica V, Sera F, Cremolini C, et al. KRAS and BRAF Mutations in Stage II and III colon cancer: a systematic review and meta-analysis. J Natl Cancer Inst. 2022;114(4):517-27. doi: https://www.doi.org/10.1093/jnci/djab190
Recebido em 13/9/2024
Aprovado em 21/2/2025
Editora-científica: Anke Bergmann. Orcid iD: https://orcid.org/0000-0002-1972-8777
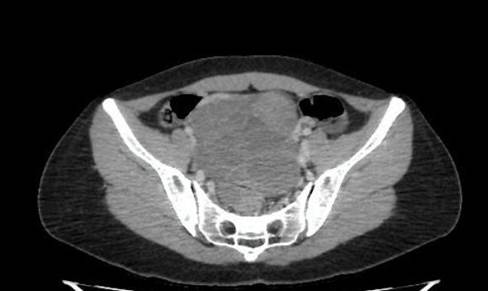
Figura 1. (31/01/2019): Volumosa lesão pélvica de aspecto cístico multiloculado, medindo aproximadamente 12,0 x 11,1 x 9,2 cm. Mantém íntimo contato com a parede anteroinferior do retossigmoide, sem plano de clivagem evidente ao método
Este é um artigo publicado em acesso aberto (Open Access) sob a licença Creative Commons Attribution, que permite uso, distribuição e reprodução em qualquer meio, sem restrições, desde que o trabalho original seja corretamente citado.