REVISÃO DE LITERATURA
Vulnerabilidade e Proteção: Revisão Integrativa da Literatura sobre o Risco Contrastante de Leucemias e Tumores Sólidos na Síndrome de Down
Vulnerability and Protection: Integrative Literature Review on the Contrasting Risk of Leukemias and Solid Tumors in Down Syndrome
Vulnerabilidad y Protección: Revisión Integradora de la Literatura sobre el Riesgo Contrastante de Leucemias y Tumores Sólidos en el Síndrome de Down
https://doi.org/10.32635/2176-9745.RBC.2026v72n1.5334
Igor Gabriel Araújo Medeiros1; Francylene Malheiros Macedo da Cunha Rego2
1,2Universidade Federal de Pernambuco (UFPE). Recife (PE), Brasil.
1E-mail: igormedeiros2@hotmail.com. Orcid iD: https://orcid.org/0009-0004-5855-6359
2E-mail: franmalheiros@hotmail.com. Orcid iD: https://orcid.org/0009-0001-3436-5337
Endereço para correspondência: Igor Gabriel Araújo Medeiros. UFPE. Avenida Professor Moraes Rego, 1235 – Cidade Universitária. Recife (PE), Brasil. CEP 50670-901. E-mail: igormedeiros2@hotmail.com
RESUMO
Introdução: A síndrome de Down (SD), caracterizada pela trissomia do cromossomo 21, está associada a risco aumentado de leucemias e redução da incidência de tumores sólidos. Objetivo: Analisar os padrões epidemiológicos e os mecanismos moleculares que explicam a susceptibilidade aumentada a leucemias e a proteção contra neoplasias sólidas em indivíduos com SD. Método: Foram selecionados 17 estudos de diferentes delineamentos, totalizando 62.121 indivíduos. Resultado: A prevalência global de câncer foi de 2,02%, sendo 1,18% de leucemias (predomínio de LLA e LMA) e 0,22% de tumores sólidos (câncer testicular como o mais comum). A razão de incidência padronizada (SIR) foi reduzida para tumores sólidos (0,69), com valores especialmente baixos para pulmão (0,10), pele (0,24) e mama (0,35). Em contrapartida, houve aumento de risco para câncer testicular (SIR: 4,28) e hepático (SIR: 3,72). Do ponto de vista molecular, a mutação GATA1 foi encontrada em praticamente todos os casos de LMA em SD, enquanto a expressão aumentada de genes supressores de tumor, como RCAN1 e DYRK1A, pode explicar a menor incidência de tumores sólidos. Conclusão: Conclui-se que a SD apresenta um perfil oncológico singular, com predisposição específica a leucemias na infância e proteção contra neoplasias sólidas, especialmente na vida adulta.
Palavras-chave: Síndrome de Down/complicações; Leucemia/epidemiologia; Neoplasias/genética; Predisposição Genética para Doença.
ABSTRACT
Introduction: Down syndrome (DS), characterized by trisomy of chromosome 21, is associated with an increased risk of leukemia and a reduced incidence of solid tumors. Objective: To analyze the epidemiological patterns and molecular mechanisms that explain the increased susceptibility to leukemias and protection against solid neoplasms in individuals with DS. Method: Seventeen studies with different designs were selected, totaling 62,121 individuals. Result: The overall prevalence of cancer was 2.02%, with 1.18% of leukemias (predominantly AML and ALL) and 0.22% of solid tumors (testicular cancer being the most common). The standardized incidence ratio (SIR) was low for solid tumors (0.69), with especially low values for lung (0.10), skin (0.24), and breast (0.35). In contrast, there was an increased risk of testicular (SIR: 4.28) and liver (SIR: 3.72) cancer. From a molecular point of view, the GATA1 mutation was found in virtually all cases of AML in DS, while increased expression of tumor suppressor genes, such as RCAN1 and DYRK1A, may explain the lower incidence of solid tumors in this population. Conclusion: It is concluded that DS presents a unique oncological profile, with a specific predisposition to leukemias in childhood and protection against solid neoplasms, especially in adulthood.
Key words: Down syndrome/complications; Leukemia/epidemiology; Neoplasms/genetics; Genetic Predisposition to Disease.
RESUMEN
Introducción: El síndrome de Down (SD), caracterizado por la trisomía del cromosoma 21, se asocia con un mayor riesgo de leucemia y una menor incidencia de tumores sólidos. Objetivo: Analizar los patrones epidemiológicos y los mecanismos moleculares que explican la mayor susceptibilidad a las leucemias y la protección contra neoplasias sólidas en individuos con SD. Método: Se seleccionaron diecisiete estudios con diferentes diseños, con un total de 62 121 individuos. Resultado: La prevalencia general de cáncer fue del 2,02%, con un 1,18% de leucemias (predominantemente LMA y LLA) y un 0,22% de tumores sólidos (siendo el cáncer testicular el más común). La razón de incidencia estandarizada (SIR) fue baja para los tumores sólidos (0,69), con valores especialmente bajos para pulmón (0,10), piel (0,24) y mama (0,35). En contraste, se observó un mayor riesgo de cáncer testicular (SIR: 4,28) y hepático (SIR: 3,72). Desde un punto de vista molecular, la mutación GATA1 se encontró en prácticamente todos los casos de LMA en el síndrome de Down, mientras que el aumento de la expresión de genes supresores de tumores, como RCAN1 y DYRK1A, podría explicar la menor incidencia de tumores sólidos. Conclusión: Se concluye que el síndrome de Down presenta un perfil oncológico único, con una predisposición específica a las leucemias en la infancia y protección contra las neoplasias sólidas, especialmente en la edad adulta.
Palabras clave: Síndrome de Down/complicaciones; Leucemia/epidemiología; Neoplasias/genética; Predisposición Genética a la Enfermedad.
INTRODUÇÃO
A síndrome de Down (SD), resultante da trissomia do cromossomo 21 (T21), é a aneuploidia mais prevalente em seres humanos, com ocorrência estimada em um a cada 600 – 1.000 nascimentos globais, e está associada a várias comorbidades clínicas, incluindo desordens hematológicas e predisposição oncológica específica1,2. Indivíduos com SD apresentam risco significativamente elevado para leucemias agudas, incluindo a leucemia megacarioblástica (LM), que engloba formas transitórias (LT) ou pré-leucêmicas, e a leucemia linfoblástica aguda (LLA), e a leucemia megacarioblástica aguda (LMA), correspondente à manifestação clínica aguda, observando-se aumento de dez a 20 vezes ou mais em comparação com crianças sem SD3.
Curiosamente, do ponto de vista epidemiológico, a incidência de tumores sólidos em pessoas com SD é notavelmente menor do que na população geral, com motivos biológicos sugerindo uma proteção intrínseca ligada à sobrecarga gênica do cromossomo 214,5. Estudos epidemiológicos robustos revelam uma prevalência global de câncer em SD em torno de 2 %, com as leucemias representando aproximadamente 1,18 % e os tumores sólidos apenas cerca de 0,22 %, sendo o câncer testicular o tipo sólido mais frequente nessa população1,4.
Uma análise abrangente envolvendo mais de 34 mil indivíduos com SD observou que a incidência de tumores sólidos nessa população gira em torno de 95 casos por 100 mil pessoas/ano. Esse número representa uma frequência consideravelmente inferior quando comparada à da população em geral. A razão de incidência padronizada (SIR) para todos os tumores sólidos foi de 0,69, com intervalo de confiança de 95% entre 0,51 e 0,94, indicando um risco substancialmente reduzido. Entre os tipos específicos de câncer com menor ocorrência, destacam-se os de mama (SIR: 0,35), pele (SIR: 0,24), pulmão (SIR: 0,10) e trato genital feminino (SIR: 0,44). Por outro lado, os dados mostraram exceções importantes: tumores localizados nos testículos e no fígado apresentaram taxas elevadas de incidência, com SIR de 4,28 e 3,72, respectivamente. Esses resultados reforçam que, embora exista um padrão de proteção contra grande parte das neoplasias sólidas, certos órgãos permanecem vulneráveis em indivíduos com T216.
Do ponto de vista molecular, a predisposição a leucemias em SD está relacionada à mutação somática em GATA1 presente em quase todos os casos de LM e na forma LT, junto a mutações adicionais em genes como JAK2 e CRLF2 em LLA5,6. A patogênese das leucemias associadas à SD envolve um modelo multietapas que começa com sobreposição de genes do cromossomo 21, seguida de mutações primárias (e.g., GATA1), rearranjos em CRLF2 e mutações em JAK2. A evolução dessas neoplasias segue o chamado modelo evolutivo somático multi-hit, no qual a T21 cria um ambiente genético permissivo, promovendo desregulação transcricional, sobre-expressão de genes e instabilidade hematopoiética. A esse contexto inicial, somam-se eventos mutacionais primários (como a mutação GATA1) e, posteriormente, alterações genéticas secundárias, que colaboram para a expansão clonal e a progressão para leucemia franca. Esse modelo implica uma trajetória evolutiva gradativa e acumulativa de eventos genéticos, característica das leucemias pediátricas associadas à SD7-10.
Por outro lado, o perfil de proteção contra tumores sólidos tem sido associado à triplicação de genes supressores de tumor, como Ets2 e RCAN1, que atuam inibindo angiogênese tumoral e promovendo regulação da apoptose e do microambiente estromal4,11. Evidências apontam, ainda, influência de microRNAs localizados na região crítica da T21, bem como alterações no sistema imunológico e metabólico, reduzindo a vulnerabilidade ao desenvolvimento tumoral em diversos órgãos4.
A compreensão detalhada das diferenças epidemiológicas e moléculas envolvidas é essencial para orientar estratégias de rastreamento personalizadas e aprimorar protocolos terapêuticos, uma vez que crianças com SD apresentam toxicidade diferencial à quimioterapia, bem como perfis prognósticos específicos, especialmente em LM com sobrevida de cinco anos superior a 90 %, e em LLA com desfechos menos favoráveis10.
Diante desse contexto, o objetivo deste estudo é reunir, sintetizar e analisar criticamente o conhecimento científico disponível sobre os riscos de leucemias e tumores sólidos em indivíduos com SD, integrando evidências oriundas de estudos com diferentes delineamentos metodológicos, buscando responder à seguinte questão de pesquisa: “quais fatores genéticos, moleculares e epidemiológicos contribuem para o aumento da predisposição a leucemias e para a aparente proteção contra tumores sólidos em indivíduos com SD?”
MÉTODO
Revisão integrativa da literatura, escolhida por possibilitar a inclusão de dados epidemiológicos quantitativos, bem como de análises teóricas e moleculares qualitativas que elucidam as particularidades oncológicas em indivíduos com SD.
A construção da revisão seguiu as seis etapas propostas por Whittemore e Knafl12: identificação do problema de pesquisa, estabelecimento dos critérios de busca, categorização dos estudos selecionados, avaliação crítica dos estudos incluídos, interpretação e síntese dos dados, e apresentação dos resultados.
A busca bibliográfica foi realizada nas seguintes bases de dados eletrônicas: PubMed/MEDLINE, Scopus, Web of Science, Embase e SciELO. Foram utilizados os seguintes descritores (em inglês e português): “Down Syndrome”, “Leukemia”, “Solid Tumors”, “Cancer”, “Neoplasms”, “Epidemiology”, “Risk”, “Genetics”, “MicroRNAs”, “Angiogenesis”, “Gene Dosage”. A inclusão de termos específicos como “MicroRNAs” e “Angiogenesis” se justificou pela necessidade de identificar estudos que investigassem os mecanismos moleculares específicos subjacentes à predisposição para leucemias e à proteção contra tumores sólidos em indivíduos com SD. Esses termos permitiram capturar evidências relacionadas à regulação genética, vias de sinalização e fatores celulares envolvidos na oncogênese diferencial nessa população.
A estratégia de busca combinou os termos usando os operadores AND e OR, conforme a estrutura PICO adaptada à revisão integrativa, considerando: População (P): indivíduos com SD; Intervenção/Exposição (I): presença de fatores genéticos, moleculares, imunológicos ou epidemiológicos associados a neoplasias; Comparador (C): população sem SD; e Desfechos (O): incidência, prevalência ou risco de leucemias e tumores sólidos, bem como suas características moleculares e clínicas.
Foram incluídos na presente revisão estudos originais, revisões sistemáticas e metanálises, publicados entre 2000 e 2025, que abordassem: incidência, prevalência ou risco relativo de leucemias e tumores sólidos em pessoas com SD; bases genéticas, moleculares ou imunológicas relacionadas a esses padrões oncológicos; estudos com amostras humanas; publicações em inglês, português ou espanhol; estudos publicados em periódicos revisados por pares.
Foram excluídos trabalhos duplicados; resumos, cartas ao editor, opiniões sem embasamento científico; estudos com amostras exclusivamente animais ou modelos celulares in vitro.
A seleção dos estudos foi realizada de forma independente por dois pesquisadores, por meio da leitura dos títulos, resumos e posteriormente dos textos completos. Divergências foram resolvidas por consenso. Os dados extraídos dos artigos incluíram: tipo de neoplasia (leucemia/tumor sólido), tipo de estudo, população-alvo, país, principais achados, fatores genéticos ou moleculares citados, e estimativas epidemiológicas como SIR ou prevalência.
Os dados foram organizados em quadros sinópticos e analisados qualitativamente, permitindo a comparação entre estudos e a identificação de padrões, lacunas e hipóteses recorrentes na literatura. Quando presente, os valores estatísticos foram apresentados conforme descritos pelos autores dos artigos, respeitando as fórmulas e os indicadores originais (IC 95%, p, OR, SIR). Nenhuma análise estatística adicional foi conduzida por este estudo.
Por se tratar de uma revisão integrativa sem envolvimento direto de seres humanos ou animais, esta pesquisa não necessitou de aprovação por um Comitê de Ética em Pesquisa (CEP), conforme previsto na Resolução n.º 510/2016 do Conselho Nacional de Saúde13. No entanto, todas as fontes utilizadas foram provenientes de publicações científicas com revisão por pares e seguiram os preceitos éticos internacionais para pesquisa.
RESULTADOS
A revisão incluiu 17 estudos com delineamentos quantitativos e qualitativos, totalizando uma amostra combinada de 62.121 indivíduos com SD. A prevalência global de câncer nessa população foi estimada em 2,02% (IC 95%: 1,63–2,50). Quanto aos desfechos primários, a prevalência de leucemias foi de 1,18% (IC 95%: 0,86–1,62), com predominância da LLA, que representou 0,86%, seguida pela LMA, com 0,51%. No que se refere aos tumores sólidos, considerados desfecho secundário, observou-se uma prevalência de 0,22% (IC 95%: 0,12–0,43), sendo o câncer testicular o tipo mais comum identificado nesse grupo14. O processo de seleção dos estudos foi conduzido conforme os critérios da revisão integrativa, iniciando-se com a identificação de 1.310 registros provenientes de cinco bases de dados: PubMed/MEDLINE (n = 410), Scopus (n = 372), Web of Science (n = 295), Embase (n = 198) e SciELO (n = 35). Após a remoção de duplicatas, 972 registros únicos foram submetidos à triagem por título e resumo, resultando na exclusão de 812 estudos que não atendiam aos critérios predefinidos. Em seguida, 160 artigos foram lidos na íntegra, dos quais 143 foram excluídos por motivos como: uso exclusivo de modelos animais ou in vitro (n = 47), ausência de dados relevantes sobre SD e câncer (n = 56), formato inadequado (cartas, editoriais) (n = 25) e dados redundantes (n = 15). Ao final, 17 estudos foram incluídos na análise qualitativa, representando o corpo final da revisão (Figura 115).
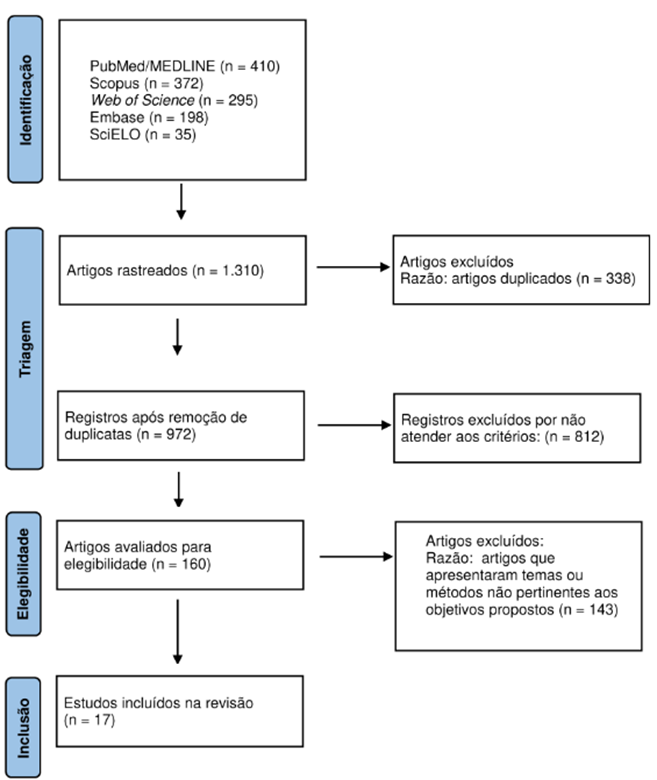
Figura 1. Fluxograma PRISMA de representação visual do processo de seleção de estudos
Fonte: Adaptado de PRISMA15.
A estimativa da SIR para tumores sólidos foi de 0,69 (IC 95% 0,51–0,94), indicando menor frequência em comparação à população geral. Especificamente, as SIR foram de 0,35 para mama, 0,24 para pele e 0,10 para pulmão. Por outro lado, aumentos de risco foram observados para tumores testiculares (SIR: 4,28; IC 95% 2,61–7,03) e hepáticos (SIR: 3,72; IC 95% 1,09–12,75)16.
Um estudo de coorte robusto conduzido com 3.530 indivíduos com SD, acompanhado por um total de 89.570 pessoas-ano, revelou padrões oncológicos distintos associados ao cariótipo e à faixa etária. A maioria dos participantes apresentava T21 clássica (92,7%), seguida por translocações Robertsonianas (4,1%) e mosaicismo (3,2%). O risco global de câncer na SD não diferiu significativamente do esperado na população geral (SIR: 0,84; IC 95%: 0,70–1,02), embora tenha sido observada uma acentuada elevação nos casos de leucemias e linfomas (SIR: 5,5; IC 95%: 4,17–7,11) e uma redução substancial no risco de tumores sólidos (SIR: 0,45; IC 95%: 0,34–0,59). Essa tendência se manteve em praticamente todos os grupos tumorais sólidos, com destaque para os cânceres de pulmão (SIR: 0,10), pele (0,24), mama (0,16) e colo do útero (0,0). Em contrapartida, o câncer testicular foi mais prevalente do que o esperado (SIR: 2,87), sendo diagnosticado em 14 homens, com predominância de seminomas entre 33 e 41 anos. O risco de leucemia, por sua vez, foi extremamente elevado em crianças menores de 5 anos, com SIR de 27 para LLA e 114 para LMA. Embora a incidência de tumores sólidos tende a se aproximar do esperado entre 15 e 30 anos, ela declina drasticamente após os 40 anos, atingindo uma SIR de 0,27 após os 50 anos. As taxas cumulativas de câncer ao longo da vida reforçam esse padrão, com incidência de leucemias atingindo 2,9% aos 60 anos em indivíduos com SD versus 0,32% na população geral, e tumores sólidos 5,0% versus 11,3%, respectivamente17.
Já Hitzler et al.18 investigaram mutações no gene GATA1, especificamente no éxon 2, em amostras de sangue periférico e medula óssea de pacientes com SD diagnosticados com leucemia LT e LMA. Foram identificadas mutações em nove de 12 pacientes com LT e em todos os três pacientes com LMA, consistindo principalmente em inserções e deleções que induzem a códons de parada prematuros, resultando em proteínas truncadas de aproximadamente 330 aminoácidos. Essas proteínas mutadas perdem o domínio de ativação transcricional da porção N-terminal, fundamental para a função normal do GATA1 durante a diferenciação eritroide e megacariocítica. A presença das mesmas mutações em amostras obtidas durante a fase de LT e após a progressão para LMA, mas ausentes após a remissão, sugere que a LMA surge da expansão clonal de células LT persistentes. Os achados sustentam o modelo evolutivo multi-hit da leucemogênese na SD, no qual a T21 fornece um contexto genético permissivo, enquanto a mutação GATA1 atua como evento iniciador, sendo posteriormente acompanhada por anomalias citogenéticas adicionais na progressão para malignidade franca. Importante destacar que essas mutações não foram encontradas em indivíduos sem SD, reforçando seu papel específico na leucemogênese associada à T21.
Em contraste com a alta incidência de leucemia infantil, os estudos mostram que a taxa de ocorrência de neoplasias em adultos com SD é consideravelmente menor, especialmente no que se refere a tumores epiteliais comuns em idades avançadas, como os de cólon, próstata e mama. Em uma análise envolvendo mulheres T21 com mais de 50 anos, nenhum caso de câncer de mama ou colorretal foi identificado, reforçando a hipótese de proteção contra carcinogênese epitelial. Dados genômicos obtidos por estudos com biópsias e análises moleculares demonstraram expressão aumentada de genes supressores tumorais localizados no cromossomo 21, como RCAN1 e DYRK1A, implicados na inibição da via de sinalização da VEGF (angiogênese), além da modulação da apoptose via NFAT (NFATC1–C4) e calcineurina. Essa expressão gênica aumentada correlaciona-se com resistência à formação de microambientes tumorais favoráveis em tecidos sólidos18.
Os resultados evidenciam que a prevalência global de câncer em indivíduos com SD foi de 2,02 %, com destaque para as leucemias (1,18 %) com baixa incidência de tumores sólidos (0,22 %)14,16. Esses dados corroboram a literatura, que aponta risco elevado para leucemias – entre dez e 20 vezes maior para LLA e até 150 vezes maior para LMA em comparação com crianças sem SD –, enquanto confirma a raridade de tumores epiteliais típicos da idade adulta. A predominância de leucemia na população analisada, com LLA em 0,86 % e LMA em 0,51 %, é consistente com estudos que descrevem um risco cumulativo em torno de 2,0 % até os 5 anos de idade e de 2,5 % até os 30 anos, reforçando o impacto clínico dessa neoplasia na SD infantile19.
A baixa incidência de tumores sólidos em indivíduos com SD, evidenciada por uma SIR global de 0,69, tem sido consistentemente demonstrada em estudos com coortes multigeracionais. Esses estudos revelam SIR ainda mais baixas para tipos específicos de câncer, como os de mama, pele e pulmão, cujas incidências são 0,35, 0,24 e 0,10, respectivamente. Em alguns casos, determinados tipos de câncer sequer foram registrados nessas populações, sugerindo uma ausência total de ocorrência. Esses dados reforçam de forma robusta a hipótese de que há um mecanismo de proteção genética específico associado à SD que confere resistência ao desenvolvimento de tumores sólidos. Tal proteção pode estar relacionada a características genéticas próprias da T21, como a superexpressão de genes com função supressora de tumor, além de alterações no microambiente celular, regulação do ciclo celular e vias de apoptose. Esses fatores parecem contribuir de maneira sinérgica para a notável redução no risco de neoplasias sólidas nessa população, contrastando com a maior suscetibilidade a certos tipos de leucemias, o que destaca a complexidade da interação entre genética e oncogênese na SD20.
Os aumentos de risco para tumores testiculares (SIR: 4,28) e hepáticos (SIR: 3,72), observados neste estudo, são coerentes com relatórios anteriores que descrevem sensibilidade aumentada de células germinativas e hepáticas em SD, sugerindo susceptibilidade seletiva nesses tecidos14,16,17. Observou-se, ainda, menor risco de tumores sólidos em adultos com mais de 50 anos, com SIR reduzida a 0,27, sem casos de câncer de mama ou colorretal, evidenciando uma possível proteção prolongada até fases tardias da vida16,19.
A ubiquidade da mutação GATA1 em casos de LMA associada à SD (LM), presente em mais de 90 % dos casos, confirma o padrão molecular característico, marcado por progressão de LT para LM na maioria dos casos até os 5 anos de idade18. A análise molecular reforça o modelo de múltiplas mutações, em que a combinação entre GATA1 e a triplicação gênica por SD é essencial para a transformação leucêmica, corroborado por estudos que identificam também alvos adicionais como JAK2 e CRLF2 em LLA19. A expressão aumentada de genes supressores de tumor como RCAN1 e DYRK1A, capazes de inibir a sinalização VEGF–calcineurina–NFAT, proporciona um mecanismo plausível para a proteção observada contra tumores sólidos, segundo experimentos em modelos murinos e iPSC humanos20.
A dualidade funcional de DYRK1A – pró-leucêmica na infância e antitumoral na vida adulta – destaca o caráter pleiotrópico desses genes, como observado por Malinge et al. em modelos murinos21 e confirmado em estudos mais amplos sobre funções imunológicas e inflamatórias ligadas ao câncer19.
Como limitações, esta revisão integrativa depende de heterogeneidade metodológica dos estudos originais, carece de dados longitudinais comparáveis e não realizou análises estatísticas próprias. Contudo, destaca-se o fortalecimento da evidência molecular e epidemiológica, apontando para estudos futuros com foco em: interações gênicas específicas em SD; longitudinalidade em coortes adultas; testes clínicos para prevenção de LM e estratégias específicas de rastreamento para câncer testicular e hepático.
CONCLUSÃO
Os achados desta revisão integrativa confirmam que a SD está associada a um perfil neoplásico único, no qual se observa uma expressiva predisposição ao desenvolvimento de leucemias agudas, principalmente na infância, e uma redução substancial na incidência de tumores sólidos. Essa constatação reforça a importância de considerar a SD não apenas como uma condição genética, mas também como um modelo de estudo para compreender mecanismos de oncogênese e resistência tumoral.
Em consonância com os objetivos propostos, foi possível identificar e quantificar os riscos relativos para diferentes tipos de cânceres em indivíduos com SD. A leucemia, especialmente a LLA e a LM, foi a neoplasia mais prevalente, enquanto tumores sólidos como mama, pulmão, pele e cólon apresentaram taxas significativamente inferiores às observadas na população geral. Os tumores testiculares e hepáticos, embora sólidos, destoam dessa tendência e apresentaram risco aumentado, indicando seletividade no padrão de suscetibilidade.
Além de descrever a distribuição epidemiológica, este estudo permitiu explorar os principais mecanismos genéticos e moleculares implicados nesse comportamento oncológico diferenciado. A mutação GATA1, virtualmente presente em todos os casos de LM, foi destacada como fator determinante para a progressão de leucemias em SD. Do mesmo modo, a superexpressão de genes localizados no cromossomo 21, como RCAN1 e DYRK1A, revelou-se central na proteção contra a formação de tumores sólidos, por inibir vias associadas à angiogênese e proliferação celular.
A presença dessas características moleculares específicas contribui para a compreensão dos processos que favorecem ou inibem o desenvolvimento de diferentes tipos de câncer, com implicações significativas para a medicina translacional. Por exemplo, compreender como a T21 atua como um mecanismo de supressão tumoral pode inspirar novas estratégias terapêuticas para outras populações, especialmente em doenças relacionadas à angiogênese e ao crescimento desregulado.
Os dados também demonstram que a faixa etária exerce influência relevante sobre os padrões neoplásicos. Crianças com SD apresentam risco extremamente elevado para leucemias, enquanto adultos, especialmente aqueles com mais de 50 anos, raramente desenvolvem neoplasias epiteliais comuns, como mama, próstata e colorretal. Isso implica a necessidade de abordagens clínicas e de rastreamento distintas ao longo da vida, com foco prioritário nas neoplasias hematológicas na infância e atenção especial para tumores testiculares e hepáticos em todas as idades.
Este estudo não apenas responde aos objetivos inicialmente traçados, mas também enfatiza a necessidade de incorporar conhecimentos genéticos no manejo clínico/oncológico de pacientes com SD. A estratificação de risco baseada em perfis moleculares pode beneficiar tanto o diagnóstico precoce quanto a personalização de protocolos terapêuticos, especialmente considerando a sensibilidade aumentada de pacientes com SD a certos agentes quimioterápicos.
Apesar de suas contribuições, esta revisão possui limitações, como a heterogeneidade dos delineamentos metodológicos dos estudos incluídos e a ausência de metanálises quantitativas. No entanto, seu caráter integrativo permitiu uma ampla análise das evidências disponíveis, favorecendo uma visão holística e atualizada sobre o tema.
Conclui-se que a SD representa um modelo natural de modulação do risco oncológico, com importantes implicações para a compreensão da biologia do câncer. Os conhecimentos aqui consolidados indicam a urgência de pesquisas futuras voltadas à caracterização genética individual, ao desenvolvimento de terapias dirigidas e ao refinamento das diretrizes clínicas para o cuidado oncológico de indivíduos com SD. Ao mesmo tempo, essas descobertas podem gerar avanços aplicáveis à população geral, especialmente no campo da prevenção e controle de tumores sólidos.
CONTRIBUIÇÕES
Igor Gabriel Araújo Medeiros contribuiu substancialmente na concepção e no planejamento do estudo; na obtenção, análise e interpretação dos dados; e na redação. Francylene Malheiros Macedo da Cunha Rego contribuiu na revisão crítica do manuscrito. Ambos os autores aprovaram a versão final a ser publicada.
DECLARAÇÃO DE CONFLITOS DE INTERESSE
Nada a declarar.
DECLARAÇÃO DE DISPONIBILIDADE DE DADOS
Todos os conteúdos subjacentes ao texto do artigo estão contidos no manuscrito.
FONTES DE FINANCIAMENTO
Não há.
REFERÊNCIAS
1. Rabin KR, Whitlock JA. Malignancy in children with trisomy 21. Oncologist. 2009;14(2):164-73. doi: https://doi.org/10.1634/theoncologist.2008-0217
2. Hasaart KAL, Bertrums EJM, Manders F, et al. Increased risk of leukaemia in children with down syndrome: a somatic evolutionary view. 2021;23:e5. doi: https://doi.org/10.1017/erm.2021.6
3. Baruchel A, Bourquin JP, Crispino J, et al. Down syndrome and leukemia: from basic mechanisms to clinical advances. Haematologica. 2023;108(10). doi: https://doi.org/10.3324/haematol.2023.283225
4. Fosu K, Quarshie JT, Sarpong KAN, et al. Inverse Comorbidity between down syndrome and solid tumors: insights from in silico analyses of down syndrome critical region genes. Genes (Basel). 2023;14(4):800. doi: https://doi.org/10.3390/genes14040800
5. Mason NR, Cahill H, Diamond Y, et al. Down syndrome-associated leukaemias: current evidence and challenges. Ther Adv Hematol. 2024;15:20406207241257901 doi: https://doi.org/10.1177/20406207241257901
6. Taherifard E, Taherifard E, Bouffet E, et al. Solid tumor incidence and patterns in individuals with down syndrome: a systematic review and meta-analysis. Pediatr Blood Cancer. 2025;72(8):e31775. doi: https://doi.org/10.1002/pbc.31775
7. Clemente AB, Ferreira BA, Carneiro LMF, et al. Risco aumentado de leucemia em crianças com síndrome de Down: mini revisão integrativa. RESU. 2024;12(supl2):179-84.
8. Gu Z, Izraeli S. All about down syndrome all. Blood. 2023;142(2):126-8. doi: https://doi.org/10.1182/blood.2023020508
9. Barwe SP, Kolb EA, Gopalakrishnapillai A. Down syndrome and leukemia: an insight into the disease biology and current treatment options. Blood Rev. 2024;64:101154. doi: https://doi.org/10.1016/j.blre.2023.101154
10. Lupo PJ, Schraw JM, Desrosiers TA, et al. Association between birth defects and cancer risk among children and adolescents in a population-based assessment of 10 million live births. JAMA Oncology. 2019;5(8):1150-8. doi: https://doi.org/10.1001/jamaoncol.2019.1215
11. Sussan TE, Yang A, Li F, et al. Trisomy represses ApcMin-mediated tumours in mouse models of down's syndrome. Nature. 2008;451:73-5. doi: https://doi.org/10.1038/nature06446
12. Whittemore R, Knafl K. The integrative review: update methodology. J Adv Nurs. 2005;52(5):546-53. doi: https://doi.org/10.1111/j.1365-2648.2005.03621.x
13. Conselho Nacional de Saúde (BR). Resolução n° 510, de 7 de abril de 2016. Dispõe sobre as normas aplicáveis a pesquisas em Ciências Humanas e Sociais cujos procedimentos metodológicos envolvam a utilização de dados diretamente obtidos com os participantes ou de informações identificáveis ou que possam acarretar riscos maiores do que os existentes na vida cotidiana, na forma definida nesta Resolução [Internet]. Diário Oficial da União, Brasília, DF. 2016 maio 24 [acesso 2025 abr 7]; Seção 1:44. Disponível em: http://bvsms.saude.gov.br/bvs/saudelegis/cns/2016/res0510_07_04_2016.html
14. Satgé D, Seidel MG. The pattern of malignancies in down syndrome and its potential context with the immune system. Front. Immunol. 2018;9(3058):1-6. doi: https://doi.org/10.3389/fimmu.2018.03058
15. Page MJ, Moher D, Bossuyt PM, et al. Prisma 2020 explanation and elaboration: updated guidance and exemplars for reporting systematic reviews. BMJ. 2021;372:n160. doi: https://doi.org/10.1136/bmj.n160
16. Moretti NR, Silva ABN, Guimarães LV, et al. The prevalence of solid tumors and hematologic malignancies among patients with down syndrome: a systematic review and meta-analysis. Crit Rev Oncol Hematol. 2025;205:104558. doi: https://doi.org/10.1016/j.critrevonc.2024.104558
17. Hasle H, Friedman JM, Olsen JH, et al. Low risk of solid tumors in persons with Down syndrome. Genet Med. 2016;18(11):1151-7. doi: https://doi.org/10.1038/gim.2016.23
18. Hitzler JK, Cheung J, Li Y, et al. GATA1 mutations in transient leukemia and acute megakaryoblastic leukemia of down syndrome. Br J Haematol. 2003;101(11):4301-4. doi: https://doi.org/10.1182/blood-2003-01-0013
19. Baek KH, Zaslavsky A, Lynch RC, et al. Down’s syndrome suppression of tumour growth and the role of the calcineurin inhibitor RCAN1. Nature. 2009;459(7250):1126-30. doi: https://doi.org/10.1038/nature08062
20. Krieg S, Krieg A, Loosen SH, et al. Risks of leukaemia and solid tumours in individuals with Down’s syndrome. Cancers. 2024;16(6):1103. doi: https://doi.org/10.3390/cancers16061103
21. Malinge S, Bliss-Moreau M, Kirsammer G, et al. Increased dosage of the chromosome 21 ortholog dyrk1a promotes megakaryoblastic leukemia in a murine model of down syndrome. J Clin Invest. 2012;122(3):948-62. doi: https://doi.org/10.1172/jci60455
Recebido em 23/6/2025
Aprovado em 25/9/2025
Editor associado: Fernando Lopes Tavares de Lima. Orcid iD: https://orcid.org/0000-0002-8618-7608
Editora-científica: Anke Bergmann. Orcid iD: https://orcid.org/0000-0002-1972-8777
Este é um artigo publicado em acesso aberto (Open Access) sob a licença Creative Commons Attribution, que permite uso, distribuição e reprodução em qualquer meio, sem restrições, desde que o trabalho original seja corretamente citado.