Miosite Ossificante Mimetizando Osteossarcoma: Relato de Caso
Myositis Ossificans Mimicking Osteosarcoma: Case Report
Miositis Osificante que Simula un Osteosarcoma: Informe de Caso
https://doi.org/10.32635/2176-9745.RBC.2025v71n4.5356
Rogério de Azevedo Hamerschmidt1; Jorge Samir Aboud2; Eduardo Morais de Castro3; Samya Hamad Mehanna4
1-4Faculdades Pequeno Príncipe. Curitiba (PR), Brasil.
1E-mail: rogeriodeazevedo04@hotmail.com. Orcid iD: https://orcid.org/0009-0004-2363-4708
2E-mail: jorge.samir.aboud21@gmail.com. Orcid iD: https://orcid.org/0009-0003-0290-8899
3E-mail: eduardo.castro@professor.fpp.edu.br. Orcid iD: https://orcid.org/0000-0001-6136-2660
4E-mail: samya.mehanna@professor.fpp.edu.br. Orcid iD: https://orcid.org/0000-0002-6636-1314
Endereço para correspondência: Rogério de Azevedo Hamerschmidt. Avenida Iguaçu 2663 – Água Verde. Curitiba (PR), Brasil. CEP 80240-031. E-mail: rogeriodeazevedo04@hotmail.com
RESUMO
Introdução: A miosite ossificante é uma condição benigna e autolimitada caracterizada pela formação óssea heterotópica nos músculos esqueléticos ou em outros locais de tecidos moles extraesqueléticos. É mais comum em adolescentes e adultos jovens fisicamente ativos. Sua incidência está relacionada com o trauma, mas pode ser desencadeada por doenças sistêmicas ou ser idiopática. Relato do caso: Paciente do sexo feminino, 48 anos, em investigação de lesão de partes moles da coxa direita, medindo 2,5 cm ao exame tomográfico, bordas mal definidas, descrita como suspeita para neoplasia, que foi submetida à biopsia e enviada a um laboratório de patologia. A amostra foi incluída para análise microscópica, sendo constituída por componente celular fusiforme exibindo atipia, sem mitoses, e com disposição em feixes. Foi descrita a presença de osteoclastos em menor quantidade, circundando o material semelhante ao osteoide. Além disso, o material foi submetido à técnica de imuno-histoquímica. Os achados favoreceram o diagnóstico de osteossarcoma. Em revisão anatomopatológica, realizada posteriormente, e incluindo estudo molecular do gene USP6, concluiu-se que se tratava de miosite ossificante mimetizando osteossarcoma. Conclusão: O diagnóstico diferencial entre osteossarcoma e miosite ossificante pode ser desafiador em virtude das semelhanças radiológicas e clínicas entre essas condições. No caso relatado, uma paciente feminina de 48 anos foi diagnosticada com osteossarcoma, porém, após reavaliação, o diagnóstico foi de miosite ossificante. Esse achado ressalta a importância da correlação entre achados clínicos, morfológicos e análises de biologia molecular para uma caracterização precisa da lesão, garantindo manejo adequado e evitando tratamentos desnecessários aos pacientes.
Palavras-chave: Miosite Ossificante/diagnóstico; Osteossarcoma/diagnóstico; Diagnóstico Diferencial; Relatos de Casos.
ABSTRACT
Introduction: Myositis ossificans is a benign, self-limiting condition characterized by heterotopic bone formation in skeletal muscles or other extra-skeletal soft tissue sites. It is most common in physically active adolescents and young adults. Its incidence is related to trauma, but it can be triggered by systemic diseases or be idiopathic. Case report: A 48-year-old female patient was investigated due to a 2.5-cm soft tissue lesion on the right thigh after tomography, with ill-defined edges, described as suspicious for neoplasia, submitted to biopsy and sent to the pathology laboratory. The sample was included for microscopic analysis, consisting of a spindle cell component showing atypia, without mitoses, and arranged in bundles. The presence of smaller quantities of osteoclasts surrounding the osteoid-like material was described. The material was also subjected to immunohistochemistry. The findings favored the diagnosis of osteosarcoma. In a later anatomopathological review, including a molecular study of the USP6 gene, it was concluded that it was myositis ossificans mimicking osteosarcoma. Conclusion: The differential diagnosis between osteosarcoma and myositis ossificans can be challenging due to the radiological and clinical similarities between these conditions. In the case reported, a 48-year-old female patient was diagnosed with osteosarcoma, but after re-evaluation, the diagnosis was myositis ossificans. This finding highlights the importance of correlating clinical and morphological findings with molecular biology analyses for accurate characterization of the lesion, ensuring appropriate management and avoiding unnecessary treatments for the patients.
Key words: Myositis Ossificans/diagnosis; Osteosarcoma/diagnosis; Diagnosis, Differential; Case Reports.
RESUMEN
Introducción: La miositis osificante es una enfermedad benigna y autolimitada que se caracteriza por la formación de hueso heterotópico en los músculos esqueléticos u otros sitios de tejido blando extraesquelético. Es más común en adolescentes y adultos jóvenes físicamente activos. Su incidencia está relacionada con traumatismos, pero puede desencadenarse por enfermedades sistémicas o ser idiopática. Informe del caso: Paciente femenina de 48 años de edad que fue investigada por una lesión de tejido blando en el muslo derecho, que medía 2,5 cm en el examen tomográfico, con bordes mal definidos, descrita como sospechosa de neoplasia, que se sometió a biopsia y se envió al laboratorio de patología. La muestra se incluyó para análisis microscópico, consistente en un componente de células fusiformes que mostraba atipia, sin mitosis y dispuestas en haces. Se describió la presencia de osteoclastos en cantidades menores, rodeando el material de aspecto osteoide. El material también fue sometido a inmunohistoquímica. Los hallazgos favorecieron el diagnóstico de osteosarcoma. En una revisión anatomopatológica posterior, que incluyó un estudio molecular del gen USP6, se concluyó que se trataba de una miositis osificante que imitaba un osteosarcoma. Conclusión: El diagnóstico diferencial entre osteosarcoma y miositis osificante puede ser complejo debido a las similitudes radiológicas y clínicas entre estas afecciones. En el caso reportado, una paciente de 48 años fue diagnosticada con osteosarcoma, pero tras una reevaluación, el diagnóstico fue miositis osificante. Este hallazgo resalta la importancia de correlacionar los hallazgos clínicos y morfológicos con los análisis de biología molecular para una caracterización precisa de la lesión, garantizar un manejo adecuado y evitar tratamientos innecesarios para los pacientes.
Palabras clave: Miositis Osificante/diagnóstico; Osteosarcoma/diagnóstico; Diagnóstico Diferencial; Informes de Casos.
INTRODUÇÃO
A miosite ossificante é uma condição benigna e autolimitada caracterizada pela formação óssea heterotópica nos músculos esqueléticos ou em outros locais de tecidos moles extraesqueléticos. É uma condição que pode surgir em qualquer idade, sendo mais comum em homens, adolescentes e adultos jovens, fisicamente ativos. Sua incidência está relacionada com o trauma, mas pode ser desencadeada por doenças sistêmicas ou ser idiopática, sendo os músculos braquial, deltoide, quadríceps e adutores os locais mais comuns, embora existam casos que tenham sido relatados em músculos intercostais, abdominais, cabeça, mãos, pés e pescoço1-3.
O quadro clínico pode apresentar desde pacientes assintomáticos até com relatos de dor, inchaço, edema em lesões superficiais, tosse, além de rigidez articular em até 20% dos casos. Pode também haver compressão de estruturas neurológicas, resultando em fraqueza, parestesia, linfedema ou até trombose venosa. A lesão tipicamente é uma massa de crescimento rápido, alcançando consolidação após dois a três meses, com diminuição dos sintomas antes de uma possível resolução. O diagnóstico por imagem pode ser preciso, com exames como a ressonância magnética com angiografia, tomografia computadorizada e ultrassonografia, especialmente nos estágios intermediário e tardio da miosite ossificante. Quando o padrão zonal típico está presente, a biópsia pode ser evitada, visto que pode ser enganosa, levando a pensar em diagnósticos diferenciais, especialmente o osteossarcoma2,4.
O diagnóstico definitivo de miosite ossificante só deve ser estabelecido após a exclusão de malignidades. Outros métodos diagnósticos incluem biópsia, imuno-histoquímica e os dados clínicos do paciente. É importante ressaltar que o diagnóstico final é realizado com a soma de todos esses componentes. O tratamento inclui anti-inflamatórios e fisioterapia para lesões precoces, e ressecção cirúrgica para casos avançados2.
O objetivo deste trabalho é relatar um caso de miosite ossificante, inicialmente diagnosticado como osteossarcoma extraesquelético, destacando características histopatológicas, imuno-histoquímicas e moleculares que permitem essa definição, além de ressaltar a importância da revisão de lâminas histopatológicas em situações de discordância diagnóstica.
Este estudo foi realizado após aprovação do Comitê de Ética em Pesquisa do Hospital Nossa Senhora das Graças, sob o número de 7.538.343 (CAAE: 87465225.7.0000.0269), em conformidade com a Lei 14.8745 de 28 de maio de 2024.
RELATO DO CASO
Paciente do sexo feminino, 48 anos, previamente hígida, com antecedente de histerectomia em maio de 2020 por miomatose uterina. Nega tabagismo ou etilismo. Sem histórico familiar de neoplasias de partes moles. Em novembro de 2024, notou aumento de volume discreto e indolor na face anterior da coxa direita, acompanhado de sensação de “peso” local. Evoluiu com dor leve intermitente, sem febre, perda de peso ou outros sintomas sistêmicos. Ao exame físico, apresentava nodulação palpável de aproximadamente 3 cm, consistência firme, não aderida a planos profundos, com discreta sensibilidade à palpação, sem sinais flogísticos. Pulsos periféricos preservados, mobilidade mantida.
A tomografia computadorizada de membros inferiores realizada após um mês evidenciou lesão de partes moles na face anterior da coxa direita, medindo 2,5 cm no maior diâmetro, com bordas mal definidas, atenuação heterogênea e realce leve e irregular após contraste, e ausência de calcificações ou erosão óssea. O aspecto foi descrito como suspeito para neoplasia de partes moles. Na sequência, foi indicada biópsia por agulha grossa guiada por ultrassonografia, realizada sem intercorrências. Os fragmentos foram encaminhados para análise histopatológica em laboratório de patologia externo. A amostra foi totalmente incluída para análise microscópica, sendo constituída por componente celular fusiforme exibindo discreta atipia, sem mitoses, e com disposição em feixes. Foi descrita a presença osteoclastos em menor quantidade, circundando o material semelhante ao osteoide.
No exame imuno-histoquímico complementar, houve negatividade para: antígeno epitelial de membrana (EMA), S100, CD34, pancitoqueratina (Pan CK), CD117, betacatenina e caldesmon. O TLE-1 foi positivo focal e o STAB2 de forma difusa. Ainda, demonstrou reação para CD68 em células gigantes multinucleadas e outras fusiformes. O índice proliferativo pelo Ki-67 foi estimado em aproximadamente 40%. A conclusão do laudo foi de que o conjunto dos achados de imuno-histoquímica, juntamente com as características clínicas e anatomopatológicas, favorecia o diagnóstico de osteossarcoma extraesquelético, sendo recomendado para avaliação definitiva a ressecção da lesão com margens de segurança para melhor análise histológica.
A paciente foi submetida a exames de estadiamento – incluindo tomografia computadorizada de tórax, abdome e pelve, bem como cintilografia óssea –, todos com resultados negativos para lesões secundárias. A partir desse diagnóstico, a paciente foi encaminhada ao médico ortopedista especialista em oncologia, em sua cidade de origem. Considerando o quadro e a necessidade de tratamento cirúrgico, foi indicada ressecção ampliada da lesão da coxa direita com margens de segurança, procedimento que poderia resultar em deformidade local e redução da mobilidade. Antes de realizá-lo, o especialista optou por revisar o caso, levantando como hipótese de diagnóstico diferencial a possibilidade de miosite ossificante. As lâminas histológicas, imuno-histoquímicas e os blocos de parafina da biópsia foram retirados e enviados a outro laboratório de patologia, para revisão com médica patologista especialista em lesões de partes moles.
Em nova análise histopatológica, descreve-se um tumor composto por proliferação de padrão fusocelular de pleomorfismo discreto, contendo células gigantes multinucleadas, focos de extravasamento de hemácias e áreas de formação de osteoide (Figura 1). Não havia focos de necrose, o índice mitótico era baixo (1 mitose/10 campos de grande aumento), não sendo identificadas mitoses atípicas.
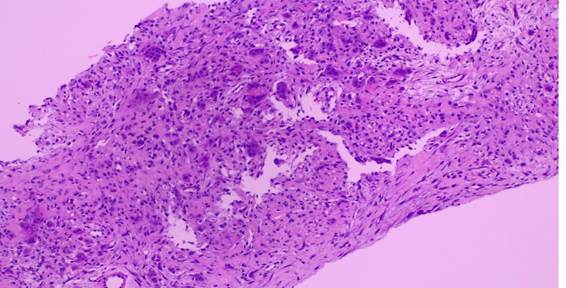
Figura 1. Proliferação de padrão fusocelular contendo células gigantes multinucleadas (microscopia óptica, hematoxilina-eosina, 100x)
Em relação à avaliação imuno-histoquímica complementar, as células de interesse demonstraram positividade para SATB2 (Figura 2A), CD68 (Figura 2B), coloração fraca e citoplasmática para betacatenina e TLE1 em raras células. E foram negativas para EMA, S100, CD34, Pan CK, CD117 e caldesmon. O índice proliferativo pelo Ki-67 foi estimado em aproximadamente 12%.
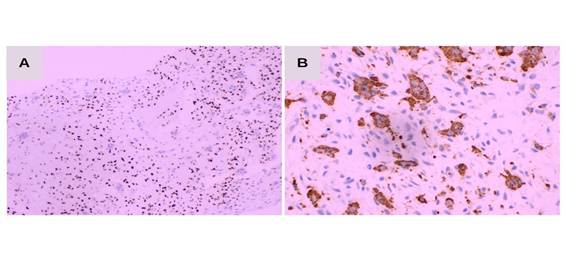
Figura 2. A: Positividade para STAB2 nas células fusocelulares (microscopia óptica, imuno-histoquímica, 40X); B: Positividade para CD68 (microscopia óptica, imuno-histoquímica, 200X)
Nesse contexto, após revisão de todo o caso, o quadro histológico e o perfil imuno-histoquímico observados sugeriram a possibilidade de miosite ossificante, embora não fosse possível avaliar adequadamente o zoneamento da lesão em razão da natureza da biópsia por agulha. A idade da paciente, a ausência de pleomorfismo, hipercromasia e mitoses atípicas reforçam essa hipótese diagnóstica.
Com base nessa hipótese, recomendou-se a realização de uma investigação molecular para o rearranjo do gene USP6, que é frequentemente presente nos casos de miosite ossificante. Adicionalmente, foi realizado estudo molecular por técnica de FISH (hibridização in situ por fluorescência) para pesquisa do gene USP6 (ubiquitina protease 6), que codifica proteína pertencente à família de enzimas de desubiquitinação. Após a desparafinação, digestão e pré-tratamento do material, o tecido foi incubado com a sonda de separação ZytoLight SPEC USP6 Dual Color Break Apart Probe (Zytovision), que contém um mix de sondas identificadas como ZyOrange e ZyGreen, que hibridizam respectivamente nas porções proximal e distal lócus do gene USP6 (17p13.2). O exame avaliou um total de 869 células e foi positivo para translocação do gene USP6 (Figura 3).

Figura 3. FISH positivo (> 10% das células) para translocação do gene USP6 (17p13.2)
Nota: A análise morfométrica quantitativa foi realizada pelo sistema analisador de imagem Metasystems Metafer acoplado a um microscópio de fluorescência Zeiss Axio Imager M1. Por causa da sua capacidade de analisar distâncias tridimensionais entre os sinais, separações gênicas podem ser detectadas em campos de interesse selecionados pelo patologista.
Diante da localização (mobilidade ainda preservada de membro inferior direito) e da gravidade dos sintomas (dor da paciente é leve), foi optado por tratamento conservador, incluindo repouso, elevação e imobilização para minimizar trauma adicional e promover a resolução espontânea da ossificação. Exercícios de amplitude de movimento e resistidos foram recomendados para melhor recuperação da função muscular e articular.
A paciente segue em acompanhamento especializado há seis meses, apresentando redução das dores, porém com poucas alterações nos exames de imagem em relação à lesão na coxa direita. Em caso de dor significativa, fraqueza muscular ou perda de movimento, poderá ser indicada cirurgia para remoção da massa óssea, sem necessidade de margens cirúrgicas de segurança e poupando a paciente de exérese ampliada.
DISCUSSÃO
A miosite ossificante é um processo benigno, não neoplásico, de ossificação heterotópica, geralmente solitário, bem encapsulado e circunscrito. É mais comumente observada nos músculos esqueléticos, mas também pode ocorrer em tendões e gordura subcutânea. É rara em lactentes e idosos, sendo mais comum em homens2,3.
A fisiopatologia da miosite ossificante não é completamente compreendida. Uma das hipóteses seria de que o trauma inicial desencadeia uma cascata inflamatória nos músculos esqueléticos, levando à liberação de citocinas. Essas citocinas atuam nas células endoteliais vasculares, causando a transição mesenquimal-endotelial. As células-tronco mesenquimais derivadas do endotélio se diferenciam em condrócitos ou osteoblastos, que, na fase final, formam osso extraesquelético. Dessa maneira, ocorrem alterações histológicas no tecido afetado, no qual se observa um núcleo central não ossificado composto por fibroblastos e miofibroblastos proliferativos, e uma pequena quantidade de osteoide e osso lamelar maduro na periferia, no estágio inicial. No estágio intermediário, predomina o componente osteoide, rodeado por uma camada de osso lamelar maduro. O estágio tardio é caracterizado pelo padrão zonal típico com uma área central de fibroblastos proliferativos e miofibroblastos, uma zona intermediária com osteoblastos e formação de osteoide imaturo e uma zona periférica de osso maduro2,4.
O diagnóstico pode ser feito por meio de exames de imagem. Os principais são a radiografia, a qual é frequentemente normal na fase inicial, podendo mostrar opacidade de tecidos moles deslocando planos de gordura. Nas fases intermediária e madura, desenvolvem-se calcificações periféricas progressivas. A ultrassonografia pode detectar a "padrão zonal" característico mais precocemente, mas sua interpretação depende da experiência do operador. A tomografia é útil para identificar calcificações precocemente e distinguir miosite ossificante de outras lesões ósseas. A ressonância magnética é a técnica de escolha para avaliar lesões de tecidos moles. No entanto, na fase inicial, a miosite ossificante pode mimetizar sarcomas de tecidos moles4.
Em relação aos achados histopatológicos em biópsias para diagnóstico, a miosite ossificante apresenta uma organização característica com um centro celular composto por células fusiformes (fibroblastos e miofibroblastos) dispostas em padrões fasciculares curtos, rodeadas por estroma frouxo e colagenoso, uma zona intermediária que exibe trabéculas ósseas imaturas cercadas por osteoblastos ativos e uma zona periférica formação óssea madura e lamelar, frequentemente associada a focos de cartilagem em ossificação endocondral. Dessa maneira, esse "padrão zonal" progressivo da periferia para o centro é diagnóstico para miosite ossificante2,4,6.
No caso relatado, para diagnóstico definitivo, foi solicitado exame imuno-histoquímico para EMA, S100, CD34, Pan CK, CD117, betacatenina, caldesmon, TLE-1 e STAB2, além do Ki-67, que indica índice proliferativo. A partir disso, a maior suspeita foi de um dos diagnósticos diferenciais da miosite ossificante, o osteossarcoma. Porém, após avaliação histoquímica complementar para o gene USP67, a história clínica do paciente e avaliação histopatológica, obteve-se diagnóstico final de miosite ossificante.
Tradicionalmente considerada uma lesão reativa, geralmente associada a trauma, a miosite ossificante é caracterizada por proliferação fibroblástica e formação de osso imaturo. No entanto, evidências recentes da literatura demonstram que a miosite ossificante faz parte de um espectro de alterações benignas associadas a rearranjos do gene USP6, compartilhando características clínicas, morfológicas e genéticas com outras entidades, como cisto ósseo aneurismático primário, fasceíte nodular e pseudotumor fibro-ósseo dos dígitos8,9.
Nesse contexto, ilustra-se a dificuldade diagnóstica desses casos em biópsias por agulha, que não trazem todos os detalhes da lesão, podendo a miosite ossificante simular tumores ósseos e de tecidos moles malignos, como osteossarcomas extraesqueléticos e sarcomas sinoviais. O diagnóstico diferencial pode ser desafiador, especialmente em fases iniciais quando exames de imagem e histopatológicos são inespecíficos. Amostras de biópsia podem conter apenas células fusiformes centrais, levando a diagnósticos errôneos4.
A paciente relatou dor leve e mobilidade do membro inferior direito preservada. Em comparação com o quadro clínico geral da miosite ossificante, os sintomas variam conforme a localização e a fase da miosite ossificante. Os pacientes geralmente apresentam dor, inchaço e edema em lesões superficiais, além de rigidez articular. O tratamento conservador é a abordagem de escolha, pois a miosite ossificante é autolimitada. Recomendam-se imobilização curta, aplicação de gelo e fisioterapia para recuperar a amplitude de movimento4.
A ressecção cirúrgica pode ser considerada em casos sintomáticos persistentes, mas deve ser postergada até que a lesão esteja completamente madura e ossificada (pelo menos 6 a 18 meses após o trauma), para minimizar o risco de recorrência10. Assim, a partir da busca pelo diagnóstico diferencial e consequente investigação, foi possível evitar a exérese ampliada em região do membro da paciente4.
CONCLUSÃO
O diagnóstico diferencial entre o osteossarcoma e a miosite ossificante pode ser desafiador em virtude das semelhanças radiológicas e clínicas entre essas condições. No caso relatado, uma paciente de 48 anos foi inicialmente diagnosticada com osteossarcoma, porém, após reavaliação detalhada e estudo molecular do gene USP6, o diagnóstico final foi de miosite ossificante. Esse achado ressalta a importância da correlação entre achados clínicos, morfológicos e análises gênicas para uma caracterização precisa da lesão, garantindo manejo terapêutico adequado e evitando tratamentos desnecessários aos pacientes.
CONTRIBUIÇÕES
Todos os autores contribuíram substancialmente na concepção e no planejamento do estudo; na obtenção, análise e interpretação dos dados; na redação e revisão crítica; e aprovaram a versão final a ser publicada.
DECLARAÇÃO DE CONFLITOS DE INTERESSE
Nada a declarar.
DECLARAÇÃO DE DISPONIBILIDADE DE DADOS
Todos os conteúdos subjacentes ao texto do artigo estão contidos no manuscrito.
FONTES DE FINANCIAMENTO
Não há.
REFERÊNCIAS
1. Koob M, Durckel J, Dosch JC, et al. Intercostal myositis ossificans misdiagnosed as osteosarcoma in a 10-year-old child. Pediatr Radiol. 2010;40(Suppl 1):S34-7. doi: https://doi.org/10.1007/s00247-010-1769-5
2. Łuczyńska E, Kasperkiewicz H, Domalik A, et al. Myositis ossificans mimicking sarcoma, the importance of diagnostic imaging – case report. Pol J Radiol. 2014;79:228-32. doi: https://doi.org/10.12659/pjr.890209
3. Rehman N, Sadashiva H, Madakshira MG, et al. Non-traumatic myositis ossificans. Autops Case Rep. 2021;11:e2021316. doi: https://doi.org/10.4322/acr.2021.316
4. Savvidou O, Papakonstantinou O, Lakiotaki E, et al. Post-traumatic myositis ossificans: a benign lesion that simulates malignant bone and soft tissue tumours. EFORT Open Rev. 2021;6(7):572-83. doi: https://doi.org/10.1302/2058-5241.6.210002
5. Ministério da Saúde (BR). Lei n.º 14.874, de 28 de maio de 2024. Dispõe sobre a pesquisa com seres humanos e institui o Sistema Nacional de Ética em pesquisa com Seres Humanos. Diário Oficial da União, Brasília, DF. 29 maio 2024 [acesso 2025 jan 14]; Seção 1:103. Disponível em: https://www.gov.br/conselho-nacional-de-saude/pt-br/camaras-tecnicas-e-comissoes/conep/legislacao/resolucoes/lei-no-114-874.pdf/view
6. Ragunanthan N, Sugavanam C. Pseudomalignant myositis ossificans mimicking osteosarcoma: a case report. J Orthop Surg (Hong Kong). 2006;14(2):219-21. doi: https://doi.org/10.1177/230949900601400224
7. Legrand M, Jourdan ML, Pinieux G. Histopathogenesis of bone- and soft-tissue tumor spectrum with USP6 gene rearrangement: multiple partners involved in the tissue repair process. Histol Histopathol. 2023;38(3):247-60. doi: https://doi.org/10.14670/hh-18-532
8. Sukov WR, Franco MF, Erickson-Johnson M, et al. Frequency of USP6 rearrangements in myositis ossificans, brown tumor, and cherubism: molecular cytogenetic evidence that a subset of "myositis ossificans-like lesions" are the early phases in the formation of soft-tissue aneurysmal bone cyst. Skeletal Radiol. 2008;37(4):321-7. doi: https://doi.org/10.1007/s00256-007-0442-z
9. Švajdler M, Michal M, Martínek P, et al. Fibro-osseous pseudotumor of digits and myositis ossificans show consistent COL1A1-USP6 rearrangement: a clinicopathological and genetic study of 27 cases. Hum Pathol. 2019;88:39-47. doi: https://doi.org/10.1016/j.humpath.2019.02.009
10. Orava S, Sinikumpu JJ, Sarimo J, et al. Surgical excision of symptomatic mature posttraumatic myositis ossificans: characteristics and outcomes in 32 athletes. Knee Surg Sports Traumatol Arthrosc. 2017;25(12):3961-8. doi: https://doi.org/10.1007/s00167-017-4667-7
Aprovado em 19/8/2025
Editora-científica: Anke Bergmann. Orcid iD: https://orcid.org/0000-0002-1972-8777
Este é um artigo publicado em acesso aberto (Open Access) sob a licença Creative Commons Attribution, que permite uso, distribuição e reprodução em qualquer meio, sem restrições, desde que o trabalho original seja corretamente citado.