Identificação de MicroRNA Associados ao Diagnóstico e Prognóstico do Colangiocarcinoma
Identification of MicroRNAs Associated with the Diagnosis and Prognosis of Cholangiocarcinoma
Identificación de MicroARNs Asociados al Diagnóstico y Pronóstico del Colangiocarcinoma
https://doi.org/10.32635/2176-9745.RBC.2026v72n1.5375
Laura Almeida Vidal1; Jamile Sofia Assis de Brito2; Lycia Lima Godoy3; Maressa de Pádua Neto Albino4; Maria Paula Alves Vilas Boas Cardoso5; Verônica Aparecida Silva Cintra6; Carlos Eduardo da Silva7; Sabrina Thalita dos Reis8
1-7Faculdade de Medicina Atenas Passos. Passos (MG), Brasil. E-mails: lauraavidal129@gmail.com; jamileassis8883@gmail.com; lycia.godoy@gmail.com; maressa.padua2@gmail.com; mpvbcardoso@gmail.com; veronicacintra17@gmail.com; carlos.silva.atenas@gmail.com. Orcid iD: https://orcid.org/0009-0000-0507-551X; Orcid iD: https://orcid.org/0009-0009-0555-6132; Orcid iD: https://orcid.org/0009-0005-9092-1421; Orcid iD: https://orcid.org/0009-0004-2206-6702; Orcid iD: https://orcid.org/0009-0008-4124-9984; Orcid iD: https://orcid.org/0009-0009-0351-3008; Orcid iD: https://orcid.org/0000-0002-1080-6660
8Universidade de São Paulo, Faculdade de Medicina. São Paulo (SP), Brasil. E-mail: sabrinareis@usp.br. Orcid iD: https://orcid.org/0000-0002-3564-3597
Endereço para correspondência: Carlos Eduardo da Silva. Rua Oscar Cândido Moreira, 1000 – Mirante do Vale. Passos (MG), Brasil. CEP 37900-380. E-mail: carlos.silva.atenas@gmail.com
RESUMO
Introdução: O colangiocarcinoma (CHOL) é uma neoplasia maligna do epitélio biliar, sendo a segunda principal forma de câncer hepático. Sua alta agressividade e diagnóstico tardio dificultam terapias eficazes. A falta de biomarcadores prognósticos confiáveis também impede o manejo clínico adequado. Nesse contexto, os microRNA (miRNA) surgem como reguladores pós-transcricionais da expressão gênica, com potencial diagnóstico e prognóstico em diversos tumores. Objetivo: Identificar os principais miRNA associados ao diagnóstico e prognóstico do CHOL, com enfoque especial na metástase linfonodal, por meio da análise bioinformática de dados obtidos do The Cancer Genome Atlas (TCGA). Método: Estudo transversal, descritivo e exploratório baseado em ferramentas de bioinformática. Foram analisadas 45 amostras (36 tumorais e 9 normais) provenientes do TCGA. Para triagem, filtragem e análise da expressão diferencial dos miRNAs em relação às variáveis clínicas e demográficas, utilizaram-se as plataformas CancerMIRNome, OncomiR e UALCAN. Resultados: Identificaram-se 245 miRNA com significância estatística, dos quais 9 demonstraram associação com a presença de metástase linfonodal: let-7c-5p, miR-1258, miR-182-5p, miR-183-5p, miR-194-3p, miR-301a-3p, miR-378a-3p, miR-92b-3p e miR-96-5p. O miR-194-3p destacou-se por sua correlação com todas as variáveis clínicas avaliadas. Não foi observada associação estatisticamente significativa entre os miRNA e a sobrevida global dos pacientes. Conclusão: Os miRNA identificados apresentam potencial para serem utilizados como biomarcadores prognósticos no CHOL, especialmente na estratificação dos pacientes com metástase linfonodal. Entretanto, são necessários estudos adicionais com validação experimental e análises funcionais para confirmar o papel desses miRNAs na progressão tumoral do CHOL.
Palavras-chave: Neoplasias Hepáticas/diagnóstico; Colangiocarcinoma/diagnóstico; MicroRNAs; Prognóstico; Biologia Computacional/estatística & dados numéricos.
ABSTRACT
Introduction: Cholangiocarcinoma (CHOL) is a malignant neoplasm of the biliary epithelium and represents the second most usual form of liver cancer. Its high aggressiveness and late diagnosis hinder the implementation of effective therapies. The lack of reliable prognostic biomarkers also impairs proper clinical management. In this context, microRNAs (miRNAs) emerge as post-transcriptional regulators of gene expression, with diagnostic and prognostic potential in various tumors. Objective: Identify key miRNAs associated with the diagnosis and prognosis of CHOL, with a particular focus on lymph node metastasis, through bioinformatic analysis of data from The Cancer Genome Atlas (TCGA). Method: A cross-sectional, descriptive, and exploratory study based on bioinformatics was conducted. A total of 45 samples (36 tumoral and 9 normal) were analyzed from TCGA. The CancerMIRNome, OncomiR, and UALCAN platforms were used for screening, filtering, and differential expression analysis of miRNAs in relation to clinical and demographic variables. Results: Two hundred forty-five miRNAs with statistical significance were identified, of which nine were associated with lymph node metastasis: let-7c-5p, miR-1258, miR-182-5p, miR-183-5p, miR-194-3p, miR-301a-3p, miR-378a-3p, miR-92b-3p, and miR-96-5p. Notably, miR-194-3p was associated with all clinical variables analyzed. No significant correlation was found between miRNA expression and overall survival. Conclusion: The identified miRNAs demonstrate potential prognostic value in CHOL, particularly for stratifying patients with lymph node metastasis. Further studies involving experimental validation and functional analyses are necessary to confirm their role in CHOL tumor progression.
Key words: Liver Neoplasms/diagnosis; Cholangiocarcinoma/diagnosis; MicroRNAs; Prognosis; Computational Biology/statistics & numerical data.
RESUMEN
Introducción: El colangiocarcinoma (CHOL) es una neoplasia maligna del epitelio biliar y constituye la segunda forma más común de cáncer hepático. Su alta agresividad y diagnóstico tardío dificultan la implementación de terapias eficaces. La falta de biomarcadores pronósticos confiables también impide un manejo clínico adecuado. En este contexto, los microARN (miARN) surgen como reguladores postranscripcionales de la expresión génica, con potencial diagnóstico y pronóstico en diversos tumores. Objetivo: Identificar los principales miARNs asociados al diagnóstico y pronóstico del CHOL, con énfasis en la metástasis ganglionar, mediante análisis bioinformático de datos del The Cancer Genome Atlas (TCGA). Método: Estudio transversal, descriptivo y exploratorio basado en bioinformática. Se analizaron 45 muestras (36 tumorales y 9 normales) extraídas del TCGA. Se utilizaron las plataformas CancerMIRNome, OncomiR y UALCAN para la selección, filtrado y análisis de la expresión diferencial de miARNs en relación con variables clínicas y demográficas. Resultados: Se identificaron 245 miARNs con significación estadística, de los cuales nueve presentaron asociación con metástasis ganglionar: let-7c-5p, miR-1258, miR-182-5p, miR-183-5p, miR-194-3p, miR-301a-3p, miR-378a-3p, miR-92b-3p y miR-96-5p. El miR-194-3p se destacó por su asociación con todas las variables clínicas analizadas. No se observó una correlación significativa con la supervivencia global de los pacientes. Conclusión: Los miARNs identificados presentan un valor pronóstico potencial en el CHOL, especialmente en la estratificación por metástasis ganglionar. No obstante, se requieren nuevos estudios con validación experimental y análisis funcionales para confirmar su papel en la progresión tumoral del CHOL.
Palabras clave: Neoplasias Hepáticas/diagnóstico; Colangiocarcinoma/diagnóstico; MicroARNs; Pronóstico; Biología Computacional/estadística & datos numéricos.
O colangiocarcinoma (CHOL) é uma neoplasia maligna originada do epitélio que reveste os ductos biliares e constitui a segunda principal forma de câncer hepático, atrás apenas do hepatocarcinoma1. Embora raro, sua incidência tem aumentado nas últimas décadas, sobretudo na forma intra-hepática2. Esse crescimento é atribuído, em parte, ao aprimoramento dos métodos diagnósticos e à maior exposição a fatores de risco, como colangite esclerosante primária, hepatolitíase, infecções parasitárias hepáticas (Clonorchis sinensis, Opisthorchis viverrini) e anomalias congênitas das vias biliares2,3. A incidência global do CHOL varia significativamente entre regiões. Nos países ocidentais, a taxa padronizada por idade situa-se entre 0,3 e 3,5 casos por 100 mil pessoas/ano, em séries de 1990 a 2018, enquanto em regiões endêmicas da Ásia pode alcançar até 85 casos por 100 mil pessoas/ano4.
Clinicamente, o CHOL é altamente agressivo e, em geral, assintomático em estádios iniciais, o que dificulta a detecção precoce. A maioria dos diagnósticos ocorre em estádios avançados, quando a ressecção cirúrgica com margens livres, principal estratégia curativa, já não é viável3. Mesmo com terapias sistêmicas, a sobrevida global permanece limitada5,6. No colangiocarcinoma intra-hepático (iCCA), a taxa em cinco anos é de cerca de 9%, podendo alcançar 40% em casos ressecáveis⁵. Após cirurgia, entretanto, os índices de recorrência seguem elevados; em uma coorte de 169 pacientes, a taxa em cinco anos foi de 74,1%, com sobrevida livre de recorrência de apenas 26,1%6. A presença de metástase linfonodal configura um dos principais fatores prognósticos, associando-se de forma consistente à menor sobrevida global e maior risco de recorrência⁷. Esses dados reforçam a necessidade de novos biomarcadores diagnósticos e prognósticos capazes de apoiar estratégias mais eficazes e individualizadas.
O estadiamento clínico do CHOL, geralmente baseado no sistema TNM modificado da American Joint Committee on Cancer, considera a extensão tumoral (T), o acometimento linfonodal (N) e a presença de metástases a distância (M), classificando os pacientes entre os estádios I e IV8. A ausência de biomarcadores eficazes para rastreamento, estratificação de risco e monitoramento terapêutico ainda representa um obstáculo central no manejo da doença9.
Nesse cenário, os microRNA (miRNA) destacam-se como reguladores pós-transcricionais da expressão gênica, modulando processos como diferenciação celular, apoptose, metabolismo e oncogênese10,11. Esses pequenos RNA não codificantes (17–25 nucleotídeos), quando desregulados por mecanismos genéticos ou epigenéticos, podem ativar vias tumorais ou inibir genes supressores, atuando como oncomiR ou supressores tumorais10,12. Sua estabilidade em tecidos e fluidos e a expressão tecido-específica conferem-lhes elevado potencial como biomarcadores diagnósticos e prognósticos13. No contexto do CHOL, estudos prévios apontam que o miR-21 e o miR-25 encontram-se diferencialmente expressos, sendo este último superexpresso em células malignas e associado à resistência à apoptose por inibir o receptor de morte 4 (DR4)14,15. Embora tais resultados sejam promissores, ainda são necessários estudos adicionais para validar esses achados e explorar novos miRNA com potencial clínico.
O avanço de ferramentas bioinformáticas aplicadas a grandes bases de dados, como o The Cancer Genome Atlas (TCGA), permitiu a identificação de miRNAs diferencialmente expressos no CHOL, favorecendo sua caracterização molecular e abrindo oportunidades para a medicina de precisão16. Apesar desses avanços, ainda há escassez de biomarcadores confiáveis para detecção precoce e estratificação prognóstica do CHOL, limitando intervenções clínicas eficazes. Diante desse cenário, o presente estudo objetivou identificar miRNA inéditos com potencial diagnóstico e prognóstico, por meio da análise integrada de dados de expressão de miRNAs e informações clínicas do TCGA-CHOL, com ênfase na associação com metástase linfonodal. Dessa forma, buscou-se contribuir para a compreensão da biologia tumoral e apontar potenciais alvos para aplicações clínicas futuras.
MÉTODO
Estudo transversal, descritivo e exploratório, com abordagem bioinformática, baseado em dados públicos e anonimizados do repositório TCGA17. Foram analisadas 45 amostras biológicas, sendo 36 provenientes de tecidos tumorais de pacientes com CHOL e 9 de tecidos normais controles, sem evidência de neoplasia, também disponibilizados pelo TCGA. Os dados moleculares empregados nesta pesquisa corresponderam a sequenciamento de RNA de miRNA (RNA-seq), previamente normalizados como Reads Per Million (RPM), o que possibilita a comparação entre amostras com diferentes profundidades de sequenciamento. O mesmo conjunto de dados tumorais e normais foi utilizado em todas as plataformas empregadas neste estudo.
O fluxo analítico iniciou-se com a triagem ampla no CancerMIRNome (versão 2.0, acessado em julho de 2024)18, um banco que integra dados do TCGA e de miRNome circulante de estudos independentes, permitindo identificar miRNA diferencialmente expressos e explorar associações com desfechos clínicos e sobrevida. Nesta etapa, foram avaliadas diferenças de expressão entre tecidos tumorais e normais, considerando variáveis clínicas como estadiamento e grau histológico, com limiar de significância de p<0,01, o que resultou na identificação de 245 miRNA diferencialmente expressos e associados a variáveis clínicas relevantes.
Em seguida, utilizou-se o OncomiR (versão 1.0, acessado em agosto de 2024)19, ferramenta voltada para análises de expressão de miRNA em câncer com base nos dados do TCGA. A triagem inicial foi conduzida por meio das plataformas CancerMIRNome e OncomiR. Pelo CancerMIRNome, identificaram-se 245 miRNA com significância estatística (p<0,01) correlacionados a variáveis clínicas e perfil de sobrevida. Posteriormente, a filtragem específica foi realizada no OncomiR, incorporando as variáveis clínicas previamente avaliadas e adicionais, como sexo, índice de massa corporal, raça dos pacientes e dados de sobrevida global. O OncomiR foi empregado em duas etapas distintas: primeiramente para validar os achados obtidos no CancerMIRNome, garantindo a consistência da expressão diferencial; em seguida, para análises estratificadas mais detalhadas no subtipo CHOL. Nessa fase, aplicaram-se testes estatísticos incluindo ANOVA e log-rank multivariado, com ajuste por False Discovery Rate (FDR), considerando significativos apenas os miRNA com p ajustado <0,01. Foram selecionados apenas os miRNA que apresentaram diferença estatisticamente significativa e se sobrepuseram em ambas as plataformas, reduzindo o conjunto inicial de 245 para 20 miRNA com relevância estatística e clínica para análises subsequentes.
O passo final do fluxo analítico foi conduzido no UALCAN (versão 2.0, acessado em setembro de 2024)20, plataforma que permite análises estratificadas da expressão gênica e de miRNA nos dados do TCGA. Os 20 miRNA intermediários foram avaliados quanto à robustez da expressão diferencial e sua associação com múltiplos parâmetros clínicos e prognósticos, incluindo tipo de amostra (tecido normal versus tumor primário), estadiamento clínico, grau histológico, status de metástase linfonodal, idade, sexo, índice de massa corporal e raça, além da análise exploratória de sobrevida global. A diferença relativa de expressão foi calculada pelo log2 fold change (log2FC), adotando-se |log2FC|>1 como critério de relevância biológica, associado a p< 0,01. Valores positivos indicaram superexpressão tumoral, enquanto valores negativos refletiram maior expressão no tecido normal. Após essa validação, foram selecionados nove miRNA finais, consistentes entre plataformas e com associação robusta aos parâmetros clínicos e prognósticos avaliados, especialmente em relação à metástase linfonodal.
Por fim, realizou-se uma análise integrativa, em que os miRNA selecionados foram confrontados com dados previamente descritos na literatura, buscando consolidar a interpretação biológica e clínica, sobretudo em relação à presença de metástase linfonodal, reconhecida como marcador prognóstico importante no colangiocarcinoma.
Considerando que a investigação se baseou exclusivamente em dados secundários, públicos, anonimizados e de livre acesso, não houve necessidade de submissão a Comitê de Ética em Pesquisa, em conformidade com a Resolução n.º 510/201621 do Conselho Nacional de Saúde e a Lei n.º 12.527/201122.
RESULTADOS
A Figura 1 apresenta a composição da amostra, com a proporção entre tecidos tumorais e normais (A), bem como a distribuição dos pacientes com CHOL segundo o estadiamento clínico (B), incluindo os estádios I a IV.
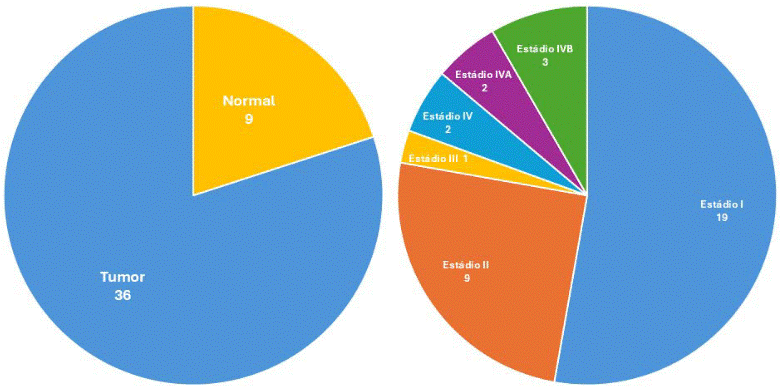
Figura 1. Representação gráfica da composição da amostra analisada neste estudo. (A) Proporção entre amostras tumorais e controles normais. (B) Distribuição dos pacientes com CHOL segundo o estadiamento clínico
Fonte: Elaborado a partir do portal TCGA17.
A triagem inicial identificou 245 miRNA diferencialmente expressos entre tecidos tumorais e normais, selecionados a partir das plataformas CancerMIRNome e OncomiR. Nas análises, foram empregados testes internos de expressão diferencial e ANOVA com correção por FDR, considerando como threshold p< 0,01 e, quando aplicável, |log2 Fold Change|>1. Esses miRNA apresentaram associação estatisticamente significativa com variáveis clínicas relevantes.
Após a filtragem específica para o subtipo CHOL (p< 0,01), foram selecionados 20 miRNA: let-7c-5p, miR-1258, miR-125b-2-3p, miR-129-5p, miR-182-5p, miR-183-5p, miR-194-3p, miR-200b-3p, miR-30c-1-3p, miR-301a-3p, miR-378a-3p, miR-4660, miR-4735, miR-4762, miR-556-3p, miR-6715a, miR-6723, miR-9-3p, miR-92b-3p e miR-96-5p. Para maior fluidez na leitura, os miRNA são referidos sem o prefixo “hsa”.
A análise de expressão diferencial, conduzida por meio da plataforma UALCAN, revelou perfis distintos de regulação gênica. A Figura 2 apresenta um gráfico de barras com os valores de log2 fold change dos miRNAs entre tecidos tumorais e normais.
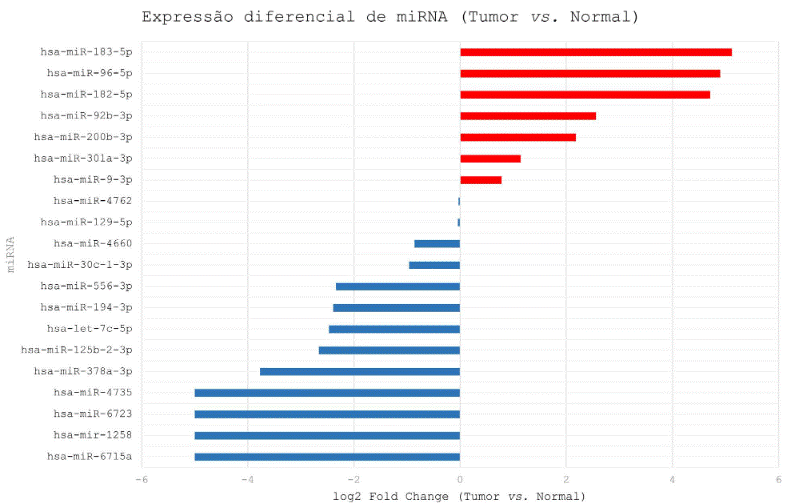
Figura 2. Gráfico de barras do log2 Fold Change (Tumor vs. Normal) para os microRNA (miRNA) analisados. Valores positivos indicam superexpressão em tecido tumoral, enquanto valores negativos correspondem a maior expressão em tecido normal. Foi adotado como cutoff biologicamente relevante |log2FC|>1
Fonte: Elaborado a partir de dados da plataforma UALCAN (TCGA)20.
Com base na análise de expressão diferencial associada à presença de metástase linfonodal, foram identificados nove miRNA com potencial relevância prognóstica no CHOL. Para isso, utilizaram-se as plataformas CancerMIRNome, OncomiR e UALCAN, sendo aplicados ANOVA com correção por FDR (OncomiR) e teste t de Student (UALCAN), considerando como threshold p<0,01. Todos os miRNA selecionados apresentaram associação estatisticamente significativa com a presença ou ausência de metástases linfonodais (p<0,01); entretanto, não foi observada correlação significativa entre seus níveis de expressão e a sobrevida global dos pacientes (p<0,05).
A Tabela 1 apresenta em detalhe os nove miRNA identificados, acompanhados dos respectivos valores de p associados às diferentes variáveis clínicas, demográficas e patológicas. Todos eles exibiram expressão diferencial significativa entre tecidos tumorais e normais (p<0,01) e demonstraram correlação com parâmetros prognósticos relevantes, incluindo estadiamento clínico, grau histológico e status de metástase linfonodal. Entre os miRNA analisados, observou-se superexpressão nos tecidos tumorais para os miRNA 182-5p, 183-5p, 301a-3p, 92b-3p e 96-5p, enquanto let-7c-5p, 1258, 194-3p e 378a-3p apresentaram níveis mais elevados nos tecidos normais.
Adicionalmente, a expressão diferencial dos miRNA manteve-se consistente entre diferentes subgrupos populacionais, abrangendo ambos os sexos, faixas etárias entre 41 e 100 anos, categorias de índice de massa corporal e, no caso específico do miR-194-3p, também entre indivíduos de diferentes etnias (caucasianos e asiáticos).
A associação significativa dos miRNA com múltiplos graus histológicos e estádios clínicos reforça a hipótese de sua participação em diferentes fases da carcinogênese biliar, desde os estádios iniciais até fases mais avançadas da doença. Entre os biomarcadores avaliados, o miR-194-3p destacou-se por apresentar significância estatística em todas as variáveis clínicas e demográficas analisadas, evidenciando-se como um candidato promissor a marcador prognóstico amplo e robusto no contexto do CHOL.
Tabela 1. MiRNA com expressão diferencial associada à metástase nodal em CHOL
|
MiRNA |
Normal x Tumor |
Estádio |
Raça |
Gênero |
Idade (anos) |
IMC |
Grau tumoral |
Metástase nodal |
Sobrevida |
|
let-7c-5p |
p<0,01 |
p<0,01 (estádios 1, 2 e 4) |
p<0,01 (cauc.)
|
p<0,01 (H=M) |
p<0,01 (41-80) |
p<0,01 (normal, sobrepeso, obesidade) |
p<0,01 (graus 2, 3 e 4) |
p<0,01 (N0, N1) |
NS |
|
miR-1258 |
p<0,01 |
p<0,01 (estádios 1, 2 e 4) |
p<0,01 (cauc.)
|
p<0,01 (H=M) |
p<0,01 (41-100) |
p<0,01 (normal, sobrepeso, obesidade) |
p<0,01 (graus 2 e 3) |
p<0,01 (N0, N1) |
NS |
|
miR-182-5p |
p<0,01 |
p<0,01 (estádios 1, 2 e 3) |
p<0,01 (cauc.)
|
p<0,01 (H=M) |
p<0,01 (41-80) |
p<0,01 (normal, sobrepeso, obesidade) |
p<0,01 (graus 2 e 3) |
p<0,01 (N0, N1) |
NS |
|
miR-183-5p |
p<0,01 |
p<0,01 |
p<0,01 (cauc.)
|
p<0,01 (H=M) |
p<0,01 (41-80) |
p<0,01 (normal, sobrepeso) |
p<0,01 (graus 2 e 3) |
p<0,01 (N0) |
NS |
|
miR-194-3p |
p<0,01 |
p<0,01 (estádios 1, 2 e 4) |
p<0,01 (cauc., asiát.) |
p<0,01 (H=M) |
p<0,01 (41-80) |
p<0,01 (normal, sobrepeso, obesidade) |
p<0,01 (graus 2, 3 e 4) |
p<0,01 (N0, N1) |
NS |
|
miR-301a-3p |
p<0,01 |
p<0,01 (estádios 1, 2 e 4) |
p<0,01 (cauc.) |
p<0,01 (H=M) |
p<0,01 (41-100) |
p<0,01 (normal, sobrepeso, obesidade) |
p<0,01 (graus 2, 3 e 4) |
p<0,01 (N0, N1) |
NS |
|
miR-378a-3p |
p<0,01 |
p<0,01 (estádios 1, 2 e 4) |
p<0,01 (cauc.)
|
p<0,01 (H=M) |
p<0,01 (41-80) |
p<0,01 (normal, sobrepeso, obesidade) |
p<0,01 (graus 2, 3 e 4) |
p<0,01 (N0, N1) |
NS |
|
miR-92b-3p |
p<0,01 |
p<0,01 (estádios 1, 2 e 4) |
p<0,01 (cauc.) |
p<0,01 (H=M) |
p<0,01 (41-80) |
p<0,01 (normal, sobrepeso) |
p<0,01 (graus 2 e 3) |
p<0,01 (N0, N1) |
NS |
|
miR-96-5p |
p<0,01 |
p<0,01 (estádios 1, 2 e 4) |
p<0,01 (cauc.)
|
p<0,01 (H=M) |
p<0,01 (41-80) |
p<0,01 (normal, sobrepeso, obesidade) |
p<0,01 (graus 2 e 3) |
p<0,01 (N0, N1) |
NS |
Fonte: Elaborado a partir de dados das plataformas CancerMIRNome, OncomiR e UALCAN (TCGA)17-20.
Legendas: IMC = índice de massa corporal; NS = não significativo; cauc. = caucasiano; asiát. = asiático; H = homens; M = mulheres, significância estatística semelhante em ambos os sexos.
Nota: Tamanho amostral: Raça: caucasianos (n=31); afro-americanos (n=1); asiáticos (n=3). Sexo: masculino (n=16); feminino (n=19). Idade: 21-40 anos (n = 2); 41-60 anos (n = 11); 61-80 anos (n=20); 81-100 anos (n=2).
DISCUSSÃO
A expressão diferencial de miRNA é amplamente reconhecida como um mecanismo epigenético central na regulação da expressão gênica, influenciando processos celulares essenciais, como proliferação, apoptose, diferenciação e migração celular10-12. Nesse contexto, os miRNA têm sido destacados como reguladores epigenéticos cruciais em diversas neoplasias, incluindo o CHOL23,24. Essas moléculas atuam predominantemente por meio do silenciamento pós-transcricional de genes-alvo, interferindo na tradução ou na estabilidade do RNA mensageiro, modulando diretamente a progressão tumoral e o comportamento biológico das neoplasias10,11.
Os achados do presente estudo revelam um conjunto de nove miRNA diferencialmente expressos com significância estatística, associados principalmente à metástase linfonodal, um marcador prognóstico de grande relevância clínica. Entre os nove explorados, sete (let-7c-5p, miR-182-5p, miR-183-5p, miR-194-3p, miR-378a-3p, miR-92a-3p e miR-96-5p) já foram correlacionados com o CHOL e os resultados deste estudo se alinham com os dados já descritos em literatura25-30. Os outros dois miRNA abordados no artigo (miR-1258 e miR-301a-3p) são inéditos, apesar de relação com outros tipos de câncer, principalmente o carcinoma hepatocelular31,32.
Nesse sentido, tais miRNA podem estar mais diretamente implicados em eventos específicos da progressão tumoral local e da disseminação linfática, exercendo influência limitada sobre desfechos clínicos de longo prazo, como a mortalidade. Entre eles destaca-se o let-7c-5p, membro da família let-7, conhecida por sua função supressora de oncogenes25. Estudos prévios demonstraram que a redução da expressão de let-7c-5p em tecidos tumorais de CHOL está associada a maior agressividade tumoral e à inibição da autorrenovação e do crescimento tumoral, embora também possa promover a invasão e crescimento em sítios extra-hepáticos, sugerindo um papel dual que depende do contexto celular e dos alvos moleculares envolvidos33. Essa dualidade pode refletir a interação com alvos distintos, como EZH2 e o eixo DVL3/β-catenina, ressaltando a complexidade de sua aplicação terapêutica33.
O miR-1258 tem sido caracterizado como supressor tumoral, inibindo a tradução da proteína RTA, reguladora da reativação de herpesvírus oncogênicos, como o associado ao sarcoma de Kaposi34. Em cânceres do trato gastrointestinal, níveis reduzidos de miR-1258 foram associados a maior estádio tumoral, comprometimento linfovascular e progressão patológica34, conferindo-lhe valor prognóstico e potencial terapêutico.
O miR-182-5p também se destaca como biomarcador terapêutico e diagnóstico, associado a mutações em genes críticos como BRCA1, BCR-ABL1 e HPGD35,36. O miRNA exossomal mir-182-5p presente na bile de pacientes com colangiocarcinoma apresentou-se superexpresso, promovendo progressão tumoral por meio da inibição do gene HPGD e consequente aumento de PGE2, evidenciando seu potencial como biomarcador e alvo terapêutico26.
O miR-183 regula vias críticas do ciclo celular, apoptose e diferenciação37,38. Em carcinomas hepáticos, pulmonares, prostáticos e colorretais, níveis elevados de miR-183 foram associados a hipermetilação do DNA, maior invasividade e pior prognóstico37,38, sugerindo sua utilidade como biomarcador e alvo terapêutico.
Nesse estudo, o miR-194-3p se destacou por sua associação com todas as variáveis clínicas e demográficas analisadas. Reconhecido como supressor tumoral em diversas neoplasias, ele regula a transição epitélio-mesenquimal (EMT), a expressão de FoxM1, PD-L1/PD-L2 e outros genes pró-tumorais39-44. Especificamente no CHOL, o miR-194-3p inibe o crescimento tumoral ao regular negativamente a sequência de transformação de células epiteliais 2 (ECT2) e bloquear a via Rho, configurando-se como um potencial alvo terapêutico27. A reintrodução desse miRNA demonstrou capacidade de inibir proliferação, migração, evasão imune e EMT em diferentes modelos, indicando seu potencial promissor para estratégias terapêuticas, inclusive em tumores quimiorresistentes39-42.
O miR-301a, por sua vez, atua predominantemente como oncomiR, inibindo supressores tumorais como RUNX3, comprometendo a função de células NK e favorecendo a proliferação tumoral45-47. Apesar de seus efeitos contextuais sobre prognóstico, neste estudo não foi observada correlação significativa entre sua expressão e a sobrevida dos pacientes.
O miR-378a-3p mostrou-se associado à supressão tumoral, inibindo RAB31 e a via Hedgehog, reduzindo proliferação, migração e a formação de células-tronco tumorais48,49. Seu desempenho como biomarcador diagnóstico e prognóstico tem sido promissor em cânceres como o de próstata.
O miR-92b-3p apresentou perfil de oncomiR, estando associado a pior prognóstico em hepatocarcinoma, câncer de mama e outras neoplasias, modulando alvos como CPEB3, ACADL e Smad750,51. Da mesma forma, o miR-96-5p, integrante do cluster miR-183, exibiu superexpressão tumoral em diversos tipos de câncer, reprimindo genes supressores como FOXO3a e PDCD4, e promovendo proliferação e sobrevivência celular52-57. Especificamente no CHOL, estudos recentes demonstram que o miR-96 exerce função oncogênica, favorecendo progressão tumoral e metástase por meio da inibição do gene MTSS1, sugerindo seu potencial como biomarcador prognóstico ou alvo terapêutico, após validação externa30.
Coletivamente, os resultados reforçam a relevância de uma abordagem integrativa que combine análises bioinformáticas e validação experimental para elucidar o papel funcional desses miRNA. Os nove miRNA diferencialmente expressos parecem atuar em processos como EMT, remodelação da matriz extracelular, evasão imune e proliferação, mecanismos centrais na disseminação linfática do CHOL. Assim, sustentam a hipótese de que esses miRNA modulam a agressividade tumoral, apresentando potencial para estratificação prognóstica de pacientes com CHOL. Embora não se tenham correlacionado com a sobrevida global, demonstraram forte associação com metástase linfonodal, um dos principais determinantes de prognóstico e elegibilidade para ressecção cirúrgica. Dessa forma, mesmo sem impacto direto sobre a mortalidade, esses miRNA podem estar mais diretamente implicados em eventos específicos da progressão tumoral local e da disseminação linfática, auxiliando na estratificação pré-operatória e na tomada de decisões terapêuticas.
Entre as limitações do estudo, destaca-se a ausência de validação experimental in vitro ou in vivo, restringindo a translação imediata dos achados para a prática clínica. Trata-se de uma análise exclusivamente bioinformática, com caráter exploratório e sem validação externa. Por outro lado, a estabilidade transdemográfica sugere que os miRNA analisados apresentam robustez biológica e clínica, sendo pouco influenciados por características individuais, o que reforça seu potencial como marcadores prognósticos. Além disso, os dados derivados exclusivamente do TCGA estão sujeitos a viés amostral e a lacunas em informações clínicas detalhadas. Futuras investigações devem contemplar a manipulação de miRNA, como o miR-194-3p e o miR-1258 em modelos celulares e murinos, bem como a validação em coortes independentes, para confirmar sua aplicabilidade como biomarcadores não invasivos ou alvos terapêuticos.
CONCLUSÃO
Este estudo identificou nove miRNAs diferencialmente expressos associados à presença de metástase linfonodal no CHOL, destacando-se o miR-194-3p por sua ampla correlação com variáveis clínicas e demográficas. Embora não tenham sido observadas associações significativas com a sobrevida global, os miRNA identificados demonstram potencial valor diagnóstico e prognóstico, sobretudo para a estratificação tumoral e a compreensão dos mecanismos moleculares subjacentes à progressão local da doença. Estudos adicionais, com validação experimental e análise funcional, são necessários para consolidar sua utilidade como biomarcadores e potenciais alvos terapêuticos no manejo do CHOL, considerando-se o caráter exploratório da presente análise.
AGRADECIMENTOS
Ao Dr. Ruan César Aparecido Pimenta pela valiosa aula sobre “Introdução à Bioinformática para Pesquisas Biomédicas com Uso de Plataformas Online”, ministrada na Liga Acadêmica de Oncologia da Faculdade Atenas Passos, a qual contribuiu para o aprofundamento dos conhecimentos aplicados neste estudo sobre miRNA no diagnóstico e prognóstico do colangiocarcinoma.
CONTRIBUIÇÕES
Todos os autores contribuíram na concepção e no planejamento do estudo; na obtenção, análise e interpretação dos dados; na redação e revisão crítica; e aprovaram a versão final a ser publicada.
DECLARAÇÃO DE CONFLITO INTERESSES
Nada a declarar.
DECLARAÇÃO DISPONIBILIDADE DE DADOS
Todos os conteúdos subjacentes ao texto do artigo estão contidos no manuscrito.
FONTES DE FINANCIAMENTO
Não há.
REFERÊNCIAS
1. Massarweh NN, El-Serag HB. Epidemiology of hepatocellular carcinoma and intrahepatic cholangiocarcinoma. Cancer Control. 2017;24(3):1073274817729245. doi: https://doi.org/10.1177/1073274817729245
2. Gomes RV. Expressão do receptor do fator de crescimento epidérmico (EGFR) como fator prognóstico no colangiocarcinoma [dissertação na Internet]. Belo Horizonte: Universidade Federal de Minas Gerais; 2016 [acesso 2025 jan 15]. 64 p. Disponível em: http://hdl.handle.net/1843/BUBD-AMNLLH
3. Banales JM, Cardinale V, Carpino G, et al. Cholangiocarcinoma: current knowledge and future perspectives consensus statement from the European Network for the Study of Cholangiocarcinoma (ENS-CCA). Nat Rev Gastroenterol Hepatol. 2016;13(5):261-80. doi: https://doi.org/10.1038/nrgastro.2016.51
4. Qurashi M, Vithayathil M, Khan SA. Epidemiology of cholangiocarcinoma. Eur J Surg Oncol. 2025;51(2):107064. doi: https://doi.org/10.1016/j.ejso.2023.107064
5. Tsung C, Quinn PL, Ejaz A. Management of intrahepatic cholangiocarcinoma: a narrative review. Cancers (Basel). 2024;16(4):739. doi: https://doi.org/10.3390/cancers16040739
6. Maki H, Kawaguchi Y, Nagata R, et al. Conditional recurrence analysis of intrahepatic cholangiocarcinoma: Changes in recurrence rate and survival after recurrence resection by disease-free interval. Hepatol Res. 2023;53(12):1224-34. doi: https://doi.org/10.1111/hepr.13951
7. Brindley PJ, Bachini M, Ilyas SI, et al. Cholangiocarcinoma. Nat Rev Dis Primers. 2021;7(1):65. doi: https://doi.org/10.1038/s41572-021-00300-2
8. Zhang XF, Xue F, Dong DD, et al. Proposed modification of the eighth edition of the AJCC staging system for intrahepatic cholangiocarcinoma. HPB (Oxford). 2021;23(5):581-591. doi: https://doi.org/10.1016/j.hpb.2020.08.016
9. Magri Júnior JE. Características anatomoclínicas e análise da sobrevida na neoplasia intraductal papilífera dos ductos biliares (IPNB) [dissertação na Internet]. Belo Horizonte: Universidade Federal de Minas Gerais; 2020 [acesso 2025 jan 15]. 45 p. Disponível em: http://hdl.handle.net/1843/46582
10. Saliminejad K, Khorram Khorshid HR, Soleymani Fard S, et al. An overview of microRNAs: biology, functions, therapeutics, and analysis methods. J Cell Physiol. 2019;234(5):5451-65. doi: https://doi.org/10.1002/jcp.27486
11. Jorge AL, Pereira ER, Oliveira CS, et al. MicroRNAs: understanding their role in gene expression and cancer. Einstein (São Paulo). 2021;19:eRB5996. doi: https://doi.org/10.31744/einstein_journal/2021RB5996
12. Hill M, Tran N. miRNA interplay: mechanisms and consequences in cancer. Dis Model Mech. 2021;14(4):dmm047662. doi: https://doi.org/10.1242/dmm.047662
13. Di Cosimo S, Appierto V, Pizzamiglio S, et al. Early modulation of circulating microRNAs levels in HER2-positive breast cancer patients treated with trastuzumab-based neoadjuvant therapy. Int J Mol Sci. 2020;21(4):1386. doi: https://doi.org/10.3390/ijms21041386
14. Bautista-Sánchez D, Arriaga-Canon C, Pedroza-Torres A, et al. The promising role of miR-21 as a cancer biomarker and its importance in RNA-based therapeutics. Mol Ther Nucleic Acids. 2020;20:409-20. doi: https://doi.org/10.1016/j.omtn.2020.03.003
15. Hussen BM, Hidayat HJ, Salihi A, et al. MicroRNA: a signature for cancer progression. Biomed Pharmacother. 2021;138:111528. doi: https://doi.org/10.1016/j.biopha.2021.111528
16. Liu X, Zhao H, Liu J, et al. Identification of tumor-suppressive miRNAs that target LAT1 expression in cholangiocarcinoma cells. Biochem Biophys Res Commun. 2024;713:1-8. doi: https://doi.org/10.1016/j.bbrc.2024.03.045
17. The Cancer Genome Atlas Program (TCGA) [Internet]. Bethesda: NIH; 2006 [acesso 2025 set 1]. Disponível em: https://www.cancer.gov/ccg/research/genome-sequencing/tcga
18. Li R, Qu H, Wang S, et al. CancerMIRNome: an interactive analysis and visualization database for miRNome profiles of human cancer. Nucleic Acids Res. 2022;50(D1):D1139-46. doi: https://doi.org/10.1093/nar/gkab784
19. OncomiR: WashU pan-cancer miRNome atlas [Internet]. St. Louis (MO): WashU; 2018 [acesso 2025 jul 1]. Disponível em: https://www.oncomir.org
20. UALCAN: TCGA miRNA analysis portal [Internet]. Birmingham:University of Alabama at Birmingham, Department of Pathology; 2017 [acesso 2025 jul 1]. Disponível em: https://ualcan.path.uab.edu
21. Conselho Nacional de Saúde (BR). Resolução n° 510, de 7 de abril de 2016. Dispõe sobre as normas aplicáveis a pesquisas em Ciências Humanas e Sociais cujos procedimentos metodológicos envolvam a utilização de dados diretamente obtidos com os participantes ou de informações identificáveis ou que possam acarretar riscos maiores do que os existentes na vida cotidiana, na forma definida nesta Resolução [Internet]. Diário Oficial da União, Brasília, DF. 2016 maio 24 [acesso 2025 abr 7]; Seção 1:44. Disponível em: http://bvsms.saude.gov.br/bvs/saudelegis/cns/2016/res0510_07_04_2016.html
22. Presidência da República (BR). Lei nº 12.527, de 18 de novembro de 2011. Regula o acesso a informações previsto na Constituição Federal. Diário Oficial da União [Internet], Brasília, DF. 2011 nov 18 [acesso 2025 abr 7]; Edição 221-A; Seção 1:1-4. Disponível em: https://pesquisa.in.gov.br/imprensa/jsp/visualiza/index.jsp?data=18/11/2011&jornal=1000&pagina=1&totalArquivos=12
23. Alkhazaali-Ali Z, Sahab-Negah S, Boroumand AR, et al. MicroRNA (miRNA) as a biomarker for diagnosis, prognosis, and therapeutics molecules in neurodegenerative disease. Biomed Pharmacother. 2024;177:116899. doi: https://doi.org/10.1016/j.biopha.2024.116899
24. He B, Zhao Z, Cai Q, et al. miRNA-based biomarkers, therapies, and resistance in cancer. Int J Biol Sci. 2020;16(14):2628-47. doi: https://doi.org/10.7150/ijbs.47203
25. Xie Y, Zhang H, Guo XJ, et al. Let-7c inhibits cholangiocarcinoma growth but promotes tumor cell invasion and growth at extrahepatic sites. Cell Death Dis. 2018;9(2):249. doi: https://doi.org/10.1038/s41419-018-0286-6
26. Shu L, Li X, Liu Z, et al. Bile exosomal miR-182/183-5p increases cholangiocarcinoma stemness and progression by targeting HPGD and increasing PGE2 generation. Hepatology. 2024;79(2):307-22. doi: https://doi.org/10.1097/HEP.0000000000000437
27. Gao J, Dai C, Yu X, et al. Upregulated microRNA-194 impairs stemness of cholangiocarcinoma cells through the Rho pathway via inhibition of ECT2. J Cell Biochem. 2020;121(10):4239-50. doi: https://doi.org/10.1002/jcb.29648
28. Zhou Z, Ma J. miR-378 serves as a prognostic biomarker in cholangiocarcinoma and promotes tumor proliferation, migration, and invasion. Cancer Biomark. 2019;24(2):173-81. doi: https://doi.org/10.3233/CBM-181980
29. Han HS, Kim MJ, Han JH, et al. Bile-derived circulating extracellular miR-30d-5p and miR-92a-3p as potential biomarkers for cholangiocarcinoma. Hepatobiliary Pancreat Dis Int. 2020;19(1):41-50. doi: https://doi.org/10.1016/j.hbpd.2019.10.009
30. Yin X, Chai Z, Sun X, et al. Overexpression of microRNA-96 is associated with poor prognosis and promotes proliferation, migration and invasion in cholangiocarcinoma cells via MTSS1. Exp Ther Med. 2020;19(4):2757-65. doi: https://doi.org/10.3892/etm.2020.8502
31. Lin W, Lin J, Li J, et al. Kindlin-2-miR-1258-TCF4 feedback loop promotes hepatocellular carcinoma invasion and metastasis. J Gastroenterol. 2022;57(5):372-86. doi: https://doi.org/10.1007/s00535-022-01866-8
32. Peng X, Yang R, Wang C, et al. The YTHDF3-DT/miR-301a-3p /INHBA axis attenuates autophagy-dependent ferroptosis in lung adenocarcinoma. Cancer Lett. 2025;613:217503. doi: https://doi.org/10.1016/j.canlet.2025.217503
33. Xie Y, Zhang H, Guo XJ, et al. Let-7c inhibits cholangiocarcinoma growth but promotes tumor cell invasion and growth at extrahepatic sites. Cell Death Dis. 2018;9:249. doi: https://doi.org/10.1038/s41419-018-0286-6
34. Shi J, Chen P, Sun J, et al. MicroRNA-1258: an invasion and metastasis regulator that targets heparanase in gastric cancer. Oncol Lett. 2017;13(5):3739-3745. doi: https://doi.org/10.3892/ol.2017.5886 Erratum in: Oncol Lett. 2021;22(6):842. doi: https://doi.org/10.3892/ol.2021.13103
35. Yacob AM, Muhamad NA, Chang KM, et al. Hsa-miR-181a-5p, hsa-miR-182-5p, and hsa-miR-26a-5p as potential biomarkers for BCR-ABL1 among adult chronic myeloid leukemia treated with tyrosine kinase inhibitors at the molecular response. BMC Cancer. 2022;22(1):332. doi: https://doi.org/10.1186/s12885-022-09396-5
36. Elias K, Smyczynska U, Stawiski K, et al. Identification of BRCA1/2 mutation female carriers using circulating microRNA profiles. Nat Commun. 2023;14(1):3350. doi: https://doi.org/10.1038/s41467-023-38925-4
37. Oliveira-Rizzo C, Ottati MC, Fort RS, et al. Hsa-miR-183-5p Modulates Cell Adhesion by Repression of ITGB1 Expression in Prostate Cancer. Noncoding RNA. 2022;8(1):11. doi: https://doi.org/10.3390/ncrna8010011
38. Li M, Xu DM, Lin SB, et al. Transcriptional expressions of hsa-mir-183 predicted target genes as independent indicators for prognosis in bladder urothelial carcinoma. Aging (Albany NY). 2022;14(9):3782-800. doi: https://doi.org/10.18632/aging.204040
39. Zhu X, Li D, Yu F, et al. miR-194 inhibits the proliferation, invasion, migration, and enhances the chemosensitivity of non-small cell lung cancer cells by targeting forkhead box A1 protein. Oncotarget. 2016;7(11):13139-52. doi: https://doi.org/10.18632/oncotarget.7545
40. Fan F, Chen K, Lu X, et al. Dual targeting of PD-L1 and PD-L2 by PCED1B-AS1 via sponging hsa-miR-194-5p induces immunosuppression in hepatocellular carcinoma. Hepatol Int. 2021;15(2):444-58. doi: https://doi.org/10.1007/s12072-020-10101-6
41. Cui Z, Wang J, Chen G, et al. The upregulation of CLGN in hepatocellular carcinoma is potentially regulated by hsa-miR-194-3p and associated with patient progression. Front Oncol. 2023;12:1081510. doi: https://doi.org/10.3389/fonc.2022.1081510
42. Vajen B, Greiwe L, Schäffer V, et al. MicroRNA-192-5p inhibits migration of triple negative breast cancer cells and directly regulates Rho GTPase activating protein 19. Genes Chromosomes Cancer. 2021;60(11):733-42. doi: https://doi.org/10.1002/gcc.22982
43. Wang Y, Huang L, Shan N, et al. Establishing a three-miRNA signature as a prognostic model for colorectal cancer through bioinformatics analysis. Aging (Albany NY). 2021;13(15):19894-907. doi: https://doi.org/10.18632/aging.203400
44. Su L, Zhang J, Zhang X, et al. Identification of cell cycle as the critical pathway modulated by exosome-derived microRNAs in gallbladder carcinoma. Med Oncol. 2021;38(12):141. doi: https://doi.org/10.1007/s12032-021-01594-8
45. Zhang J, Yang Y, Wei Y, et al. Hsa-miR-301a-3p inhibited the killing effect of natural killer cells on non-small cell lung cancer cells by regulating RUNX3. Cancer Biomark. 2023;37(4):249-59. doi: https://doi.org/10.3233/cbm-220469
46. Öztemur Islakoğlu Y, Noyan S, Gür Dedeoğlu B. Hsa-miR-301a- and SOX10-dependent miRNA-TF-mRNA regulatory circuits in breast cancer. Turk J Biol. 2018;42(2):103-12. doi: https://doi.org/10.3906/biy-1708-17
47. Pliakou E, Lampropoulou DI, Dovrolis N, et al. Circulating miRNA expression profiles and machine learning models in association with response to irinotecan-based treatment in metastatic colorectal cancer. Int J Mol Sci. 2022;24(1):46. doi: https://doi.org/10.3390/ijms24010046
48. Xu X, Li Y, Liu G, et al. MiR-378a-3p acts as a tumor suppressor in gastric cancer via directly targeting RAB31 and inhibiting the Hedgehog pathway proteins GLI1/2. Cancer Biol Med. 2022;19(12):1662-82. doi: https://doi.org/10.20892/j.issn.2095-3941.2022.0337
49. Zhang Y, Ding N, Xie S, et al. Identification of important extracellular vesicle RNA molecules related to sperm motility and prostate cancer. Extracell Vesicles Circ Nucleic Acids. 2021;2(2):104-26. doi: https://doi.org/10.20517/evcna.2021.02
50. Deng R, Cui X, Dong Y, et al. Construction of circRNA-Based ceRNA network to reveal the role of circRNAs in the progression and prognosis of hepatocellular carcinoma. Front Genet. 2021;12:626764. doi: https://doi.org/10.3389/fgene.2021.626764
51. Manzanarez-Ozuna E, Flores DL, Gutiérrez-López E, et al. Model based on GA and DNN for prediction of mRNA-Smad7 expression regulated by miRNAs in breast cancer. Theor Biol Med Model. 2018;15(1):24. doi: https://doi.org/10.1186/s12976-018-0095-8
52. Hong Y, Liang H, Uzair-ur-Rehman, et al. miR-96 promotes cell proliferation, migration and invasion by targeting PTPN9 in breast cancer. Sci Rep. 2016;6:37421. doi: https://doi.org/10.1038/srep37421
53. Mendes DCC, Calvano Filho CMC, Garcia N, et al. Could FOXO3a, miR-96-5p, and miR-182-5p be useful for Brazilian women with luminal a and triple-negative breast cancers prognosis and target therapy? Clinics (Sao Paulo). 2023;78:e100155. doi: https://doi.org/10.1016/j.clinsp.2022.100155
54. Kandhavelu J, Subramanian K, Khan A, et al. Computational analysis of miRNA and their gene targets significantly involved in colorectal cancer progression. Microrna. 2019;8(1):68-75. doi: https://doi.org/10.2174/2211536607666180803100246
55. Gujrati H, Ha S, Wang BD. Deregulated microRNAs involved in prostate cancer aggressiveness and treatment resistance mechanisms. Cancers (Basel). 2023;15(12):3140. doi: https://doi.org/10.3390/cancers15123140
56. Ma Y, Liang AJ, Fan YP, et al. Dysregulation and functional roles of miR-183-96-182 cluster in cancer cell proliferation, invasion and metastasis. Oncotarget. 2016;7(27):42805-25. doi: https://doi.org/10.18632/oncotarget.8715
57. Zheng Y, Sukocheva O, Tse E, et al. MicroRNA-183 cluster: a promising biomarker and therapeutic target in gastrointestinal malignancies. Am J Cancer Res [Internet]. 2023 [acesso 2025 nov 17];13(12):6147-75. Disponível em: https://pubmed.ncbi.nlm.nih.gov/38187051/
Recebido em 23/7/2025
Aprovado em 5/10/2025
Editora associada: Tatiana de Almeida Simão. Orcid iD: https://orcid.org/0000-0001-8509-2247
Editora-científica: Anke Bergmann. Orcid iD: https://orcid.org/0000-0002-1972-8777
Este é um artigo publicado em acesso aberto (Open Access) sob a licença Creative Commons Attribution, que permite uso, distribuição e reprodução em qualquer meio, sem restrições, desde que o trabalho original seja corretamente citado.