Mortalidade por Câncer Colorretal nos Países dos BRICS de 1990 a 2019: Análise de Idade-Período-Coorte
Colorectal Cancer Mortality in the BRICS Countries from 1990 to 2019: Age-Period-Cohort Analysis
Mortalidad por Cáncer Colorrectal en los Países BRICS de 1990 a 2019: Análisis de Cohortes por Periodos de Edad
https://doi.org/10.32635/2176-9745.RBC.2026v72n1.5403
Marcus Verly-Miguel1; Caroline Madalena Ribeiro2
1Universidade do Estado do Rio de Janeiro (Uerj), Instituto de Medicina Social Hesio Cordeiro (IMS). Rio de Janeiro (RJ), Brasil. Universidade NOVA de Lisboa, Global Health and Tropical Medicine (GHTM), Instituto de Higiene e Medicina Tropical (IHMT). Lisboa, Portugal. E-mail: miguel.marcus@ya.ru. Orcid iD: https://orcid.org/0000-0001-7347-7852
2Instituto Nacional de Câncer (INCA), Coordenação de Prevenção e Vigilância (Conprev), Divisão de Detecção Precoce e Apoio à Organização de Rede. Rio de Janeiro (RJ), Brasil. E-mail: cribeiro@inca.gov.br. Orcid iD: https://orcid.org/0000-0003-2690-5791
Endereço para correspondência: Marcus Verly-Miguel. Uerj. Rua São Francisco Xavier, 524, Bloco E, 7º andar – Maracanã. Rio de Janeiro (RJ), Brasil. CEP 20550-013. E-mail: miguel.marcus@ya.ru
RESUMO
Introdução: O câncer colorretal (CCR) é responsável por mais de 900 mil óbitos anuais no mundo, com diferenças regionais marcantes. Objetivo: Analisar a evolução da mortalidade por CCR nos países membros originais do BRICS entre 1990 e 2019 e estimar os efeitos de idade, período e coorte. Método: Estudo ecológico de séries temporais da mortalidade por CCR em adultos de 30 a 69 anos, utilizando dados do Global Burden of Disease 2019. Os efeitos de idade, período e coorte foram analisados utilizando a ferramenta Age-Period-Cohort Analysis Tool do Instituto Nacional do Câncer dos Estados Unidos. Resultados: Observou-se aumento da mortalidade entre 1990 e 2019 em todos os países do BRICS. O efeito de idade foi identificado em todos os países, com maiores taxas em faixas etárias mais avançadas. Quanto à coorte de nascimento, observaram-se aumento constante na mortalidade masculina no Brasil, China e Índia, e diminuição na mortalidade feminina na China e na Rússia. Conclusão: A análise idade-período-coorte demonstrou que o acréscimo da mortalidade se concentra sobretudo em homens pertencentes a coortes pós-1960 e em faixas etárias economicamente ativas, ao passo que a Rússia exemplifica o potencial de políticas de controle para reverter a tendência. Os resultados apontaram para um aumento nas taxas de mortalidade por CCR em todos os países originais do BRICS, embora esse crescimento não ocorra de maneira uniforme.
Palavras-chave: Neoplasias Colorretais/mortalidade; Mortalidade/tendências; Estudos de Coortes.
ABSTRACT
Introduction: Colorectal cancer (CRC) is responsible for over 900,000 deaths annually worldwide, with marked regional differences. Objective: To analyze the trends in CRC mortality in BRICS countries between 1990 and 2019, and to estimate the effects of age, period, and cohort. Method: An ecological time series study of CRC mortality in adults aged 30 to 69 years, using data from the “Global Burden of Disease 2019”. Age-period-cohort effects were analyzed using the “Age-Period-Cohort Analysis Tool” developed by the United States National Cancer Institute. Results: An increase in mortality was observed between 1990 and 2019 in all BRICS countries. An age effect was identified in all countries, with higher rates in older age groups. Regarding birth cohort, a steady increase in male mortality was observed in Brazil, China and India, and a decrease in female mortality in China and Russia. Conclusion: The age-period-cohort analysis showed that the increase in mortality is mainly concentrated among men born after 1960 and within economically active age groups, while Russia illustrates the potential of control policies to reverse this trend. The results indicated a rise in CRC mortality rates in all founding BRICS countries, although this growth did not occur uniformly.
Key words: Colorectal Neoplasms/mortality; Mortality/trends; Cohort Studies.
RESUMEN
Introducción: El cáncer colorrectal (CCR) es responsable de más de 900 000 muertes anuales en el mundo, con marcadas diferencias regionales. Objetivo: Analizar la evolución de la mortalidad por CCR en los países BRICS entre 1990 y 2019, y estimar los efectos de edad, período y cohorte. Método: Estudio ecológico de series de tiempo de la mortalidad por CCR en adultos de 30 a 69 años, utilizando datos del Global Burden of Disease 2019. Los efectos de edad, período y cohorte fueron analizados utilizando la herramienta Age-Period-Cohort Analysis Tool del Instituto Nacional del Cáncer de los Estados Unidos. Resultados: Se observó un aumento de la mortalidad entre 1990 y 2019 en todos los países BRICS. El efecto de la edad fue identificado en todos los países, con tasas más altas en los grupos etarios de mayor edad. En cuanto a la cohorte de nacimiento, se observaron un aumento constante en la mortalidad masculina en Brasil, China e India, y una disminución en la mortalidad femenina en China y Rusia. Conclusión: El análisis de edad-período-cohorte demostró que el aumento de la mortalidad se concentra sobre todo en hombres pertenecientes a cohortes nacidas después de 1960 y en grupos de edad económicamente activos, mientras que Rusia ejemplifica el potencial de las políticas de control para revertir la tendencia. Los resultados señalaron un aumento en las tasas de mortalidad por CCR en todos los países originales BRICS, aunque este crecimiento no se presenta de manera uniforme.
Palabras clave: Neoplasias Colorrectales/mortalidad; Mortalidad/tendencias; Estudios de Cohortes.
INTRODUÇÃO
O câncer colorretal (CCR) é a terceira neoplasia mais incidente e a segunda causa de morte por câncer, provocando mais de 900 mil óbitos anuais no mundo1. Nos países de alta renda, o rastreamento regular e os avanços cirúrgicos, radioterápicos e quimioterápicos reduziram a mortalidade nas últimas décadas. No entanto, observa-se crescimento acelerado do CCR em nações de renda média, impulsionado por urbanização, transição nutricional e envelhecimento populacional2,3.
Entre essas nações, destacam-se os países originais do bloco BRICS – Brasil, Rússia, Índia, China e África do Sul – que reúnem cerca de 40% da população global, economias em rápida expansão e profundas mudanças demográficas e de estilo de vida1,4. Esses países respondem hoje por 42% das mortes por câncer e, em 2012, perderam 46,3 bilhões de dólares em produtividade (0,33% do PIB coletivo) em razão de óbitos prematuros por neoplasias5.
A maior parte das publicações sobre CCR nos países do BRICS baseia-se em séries temporais nacionais ou revisões focadas em um único país6-9. Por outro lado, análises comparativas globais reúnem países com grande heterogeneidade de renda, estrutura etária, cobertura de rastreamento e qualidade dos registros, sem recorte específico para o BRICS, o que limita a transferência direta de políticas entre contextos semelhantes1,2,5,10,11. Mapear em conjunto a mortalidade por CCR nos países originais do BRICS pode acelerar o intercâmbio de estratégias para enfrentar fatores de risco em ascensão, como dietas ricas em ultraprocessados, sedentarismo e obesidade3,12, além de iluminar desigualdades internas no acesso ao rastreamento e ao tratamento.
O Global Burden of Disease (GBD) 2019 disponibiliza séries anuais harmonizadas de mortalidade por CCR de 1990 a 2019, baseadas em registros de óbito, censos populacionais e ajustes para sub-registro13. Esses dados permitem aplicar o modelo idade-período-coorte (APC), que decompõe as variações nas taxas em efeitos do ciclo de vida (idade), de mudanças históricas (período) e de experiências geracionais (coorte)14. A abordagem identifica grupos de maior risco, avalia o impacto temporal de políticas públicas e orienta a alocação de recursos. Como referência externa, utilizou-se a categoria “Países de Alta Renda da América do Norte”, composta por Estados Unidos, Canadá e Groenlândia.
Diante desse contexto, o objetivo deste estudo é analisar a evolução das taxas padronizadas de mortalidade por CCR nos países originais do BRICS entre 1990 e 2019 e estimar os efeitos de idade, período e coorte sobre essas tendências.
MÉTODO
Os dados foram obtidos do GBD 2019, que estima mortalidade, morbidade e fatores de risco em escala mundial13. Desenvolvido pelo Institute for Health Metrics and Evaluation da Universidade de Washington, o GBD fornece estimativas detalhadas sobre a mortalidade, morbidade e impacto das principais doenças, lesões e fatores de risco na saúde da população global13. Os dados estão disponíveis on-line15.
Para cada país, coletaram‑se o número anual de óbitos por CCR (CID‑10, C18–C21) e as taxas de mortalidade padronizadas por idade (ASR) nos grupos etários de 30‑34 até 65‑69 anos, no período 1990‑2019. Foram incluídos os cinco países membros originais do BRICS (Brasil, Rússia, Índia, China e África do Sul) e, como referência externa, o agregado de países de alta renda da América do Norte (Estados Unidos, Canadá e Groenlândia).
O BRICS reúne grandes economias emergentes em acelerada transição demográfica e nutricional, compartilhando tendência de aumento de doenças crônicas não transmissíveis3,13. Comparar internamente o bloco permite examinar como diferentes sistemas de saúde, níveis de cobertura de rastreamento e padrões de risco modificam a mortalidade por CCR.
Os dados de países de alta renda da América do Norte foram selecionados para comparação, considerando que estes já passaram pelo processo de transição demográfica e epidemiológica, possuem melhor acesso a programas de rastreamento e tratamento desse câncer e recentemente apresentaram taxas de incidência e mortalidade inferiores às dos países de média renda1, configurando um parâmetro comparativo para avaliar a distância entre as trajetórias do BRICS e um cenário considerado de máximo controle possível16. A Groenlândia integra a categoria por convenção metodológica do GBD e, em razão de seu reduzido contingente populacional, exerce impacto numérico mínimo sobre o agregado.
Os dados populacionais correspondem às projeções oficiais das Nações Unidas, disponíveis on-line17.
Trata-se de um estudo ecológico de séries temporais de mortalidade por CCR em adultos de 30 a 69 anos, faixa que concentra a maioria dos óbitos e evita instabilidade de registros nos extremos etários. O modelo IPC incluiu parâmetros que descrevem as relações matemáticas entre a taxa de mortalidade por CCR e a idade dos indivíduos, o período do diagnóstico e a coorte de nascimento, na população geral e estratificado por sexo18,19.
No modelo IPC, o net drift
representa a tendência log-linear por período e coorte para toda a população e
o local drift representa a tendência log-linear por período e coorte
para cada faixa etária20. Para o cálculo da mortalidade por idade e
período, foi realizado o agrupamento quinquenal (entre 1990 e 2019). As
estimativas do modelo foram executadas na ferramenta on-line Age Period
Cohort Analysis Tool, desenvolvida pelo National Cancer Institute
dos Estados Unidos, disponível on-line21. Para examinar a
significância dos parâmetros e funções estimáveis, foi utilizado o teste Wald ![]() .
.
O estudo utilizou exclusivamente bases secundárias, de domínio público e sem identificação individual. De acordo com a Resolução n.º 510/201622 do Conselho Nacional de Saúde do Brasil, pesquisas dessa natureza são isentas de apreciação por Comitê de Ética.
RESULTADOS
A Tabela 1 e a Figura 1 mostram que, entre 1990 e 2019, a taxa de mortalidade padronizada por idade (TMPI) por CCR caiu 33% nos países de alta renda da América do Norte, mas subiu cerca de 25% no conjunto dos BRICS. Em 2019, o bloco concentrava 41,5% da população mundial e 38,3% dos óbitos globais por CCR, com TMPI média de 11,1 por 100 mil habitantes contra 13,2 nos países de referência.
As trajetórias internas foram heterogêneas. A Rússia manteve as maiores TMPI, porém as reduziu após 2000. China e Índia concentraram o acréscimo absoluto de óbitos, com elevações relativas de 26 % e 27 %. O Brasil teve aumento moderado (12 %) seguido de estabilização, enquanto a África do Sul permaneceu praticamente estável, com discreto declínio entre mulheres.
As diferenças por sexo foram marcantes. Todas as nações do BRICS registraram crescimento mais rápido entre homens, sobretudo a China. Nos países de alta renda, as TMPI caíram em proporções semelhantes entre homens e mulheres, mantendo-se, ainda assim, em níveis absolutos superiores aos do bloco emergente (Tabela 1).
Tabela 1. Características populacionais e da mortalidade por câncer colorretal nos países membros originais do BRICS entre 1990 e 2019
|
|
BRICS |
|
Brasil |
|
|
|
1990 |
2019 |
1990 |
2019 |
|
População |
|
|
|
|
|
Total (milhões) |
2.360 |
3.223 |
150 |
211 |
|
Porcentagem global |
44,39% |
41,51% |
2,81% |
2,72% |
|
Masculina (milhões) (%) |
1.198 (50,85) |
1.639 (50,96) |
74 (49,66) |
104 (49,29) |
|
Feminina (milhões) (%) |
1.158 (49,15) |
1.577 (49,03) |
75 (50,34) |
107 (50,71) |
|
Câncer colorretal |
|
|
|
|
|
Óbitos |
141.359 |
415.359 |
8.340 (7.991; 8.610) |
27.051 (25.084; 28.402) |
|
Óbitos masculinos |
70.306 |
237.355 |
3.940 (3.779; 4.086) |
13.406 (12.520; 14.212) |
|
Óbitos femininos |
71.049 |
178.002 |
4.399 (4.165; 4.575) |
13.645 (12.369; 14.593) |
|
Proporção relativa* |
6,26% |
9,73% |
7,09% |
10,17% |
|
Proporção masculina |
5,31% |
9,32% |
6,16% |
9,40% |
|
Proporção feminina |
7,62% |
10,35% |
8,20% |
11,05% |
|
TMPI** |
8,86 |
11,14 |
10,21 (9,68; 10,57) |
11,67 (10,81; 12,28) |
|
TMPI masculino |
9,87 |
13,80 |
10,32 (9,79; 10,72) |
13,09 (12,14; 13,88) |
|
TMPI feminino |
8,25 |
9,13 |
10,07 (9,40; 10,52) |
10,52 (9,54; 11,25) |
|
|
Rússia |
|
Índia |
|
|
|
1990 |
2019 |
1990 |
2019 |
|
População |
|
|
|
|
|
Total (milhões) |
148 |
150 |
870 |
1383 |
|
Porcentagem global |
2,78% |
1,88% |
16,20% |
17,73% |
|
Masculina (milhões) (%) |
69 (46,94) |
67 (46,21) |
449 (52,12) |
714 (51,67) |
|
Feminina (milhões) (%) |
78 (53,06) |
78 (53,79) |
420 (48,78) |
668 (48,33) |
|
Câncer colorretal |
|
|
|
|
|
Número total de óbitos |
29.696 (28.698; 30.770) |
42.834 (37.637; 48.395) |
21.971 (19.161; 25.094) |
79.097 (67.137; 92.723) |
|
Óbitos em homens |
12.151 (11.670; 12.669) |
19.267 (15.992; 22.930) |
11.225 (9.579; 14.024) |
37.614 (29.868; 46.220) |
|
Óbitos em mulheres |
17.544 (16.897; 18.482) |
23.567 (19.759; 27.651) |
10.745 (8.563; 13.329) |
41.483 (32.822; 50.946) |
|
Proporção relativa* |
10,76% |
14,43% |
5,83% |
8,48% |
|
Proporção masculina |
8,08% |
12,38% |
5,55% |
8,00% |
|
Proporção feminina |
13,96% |
16,70% |
6,16% |
8,97% |
|
TMPI** |
16,71 (16,11; 17,33) |
18,17 (15,96; 20,54) |
5,47 (4,77; 6,25) |
7,50 (6,35; 8,76) |
|
TMPI masculino |
21,62 (20,83; 22,53) |
23,10 (19,25; 27,29) |
5,48 (4,61; 6,84) |
7,42 (5,92; 9,05) |
|
TMPI feminino |
14,80 (14,24; 15,61) |
15,46 (12,88; 18,23) |
5,47 (4,30; 6,84) |
7,58 (6,02; 9,26) |
|
|
China |
|
África do Sul |
|
|
|
1990 |
2019 |
1990 |
2019 |
|
População |
|
|
|
|
|
Total (milhões) |
1153 |
1421 |
39 |
58 |
|
Porcentagem global |
21,52% |
18,29% |
0,74% |
0,74% |
|
Masculina (milhões) (%) |
587 (51,36) |
726 (51,09) |
19 (48,72) |
28 (49,12) |
|
Feminina (milhões) (%) |
565 (49,43) |
695 (48,91) |
20 (51,28) |
29 (50,88) |
|
Câncer colorretal |
|
|
|
|
|
Número de óbitos |
79.322 (69.661; 89.294) |
261.776 (224.403; 303.317) |
2.030 (1.721; 2.491) |
4.601 (4.159; 5.197) |
|
Óbitos masculinos |
42.023 (34.898; 49.395) |
164.729 (132.244; 202.320) |
967 (809; 1.255) |
2.339 (2.084; 2.700) |
|
Óbitos femininos |
37.298 (31.305; 43.321) |
97.046 (78.376; 117.167) |
1.063 (870; 1.310) |
2.261 (1.966; 2.594) |
|
Proporção relativa* |
5,44% |
9,64% |
7,32% |
8,40% |
|
Proporção masculina |
4,70% |
9,42% |
6,58% |
8,16% |
|
Proporção feminina |
6,59% |
10,03% |
8,15% |
8,65% |
|
TMPI** |
10,18 (9,03; 11,37) |
13,86 (11,92; 16,01) |
10,39 (8,75; 12,96) |
11,21 (10,13; 12,60) |
|
TMPI masculino |
11,73 (9,95; 13,59) |
19,32 (15,80; 23,15) |
11,65 (9,72; 15,36) |
14,01 (12,56; 15,98) |
|
TMPI feminino |
9,14 (7,73; 10,58) |
9,68 (7,82; 11,68) |
9,38 (7,60; 11,71) |
9,31 (8,10; 10,64) |
Legendas: * = Proporção em comparação a todos os tipos de neoplasia (mortes por câncer colorretal/mortes por todas as neoplasias); ** = Taxa de mortalidade por câncer colorretal por 100 mil habitantes padronizada por idade.
A Figura 1 destaca trajetórias divergentes ao longo de três décadas. Nos países de alta renda da América do Norte, as TMPI e a participação do CCR entre todas as neoplasias caíram continuamente até meados dos anos 2000, estabilizando-se em patamar inferior. No BRICS, as trajetórias foram heterogêneas: China e Índia exibiram aumentos persistentes; o Brasil subiu até 2005 e estagnou; a Rússia passou de um pico no início dos anos 1990 para declínio sustentado desde 2000; e a África do Sul permaneceu próxima da estabilidade, com leve alta nos homens.
A mortalidade proporcional por CCR aumentou em todo o BRICS, mais acentuadamente na China, sobretudo entre o fim dos anos 1990 e início de 2010. O Brasil elevou-se até meados dos anos 2000 e estabilizou. Nas economias de alta renda, a proporção relativa diminuiu quase linearmente entre 1990 e 2005 e permaneceu estável, refletindo avanços no controle de outros tumores e no rastreamento e tratamento do CCR (Figura 1).
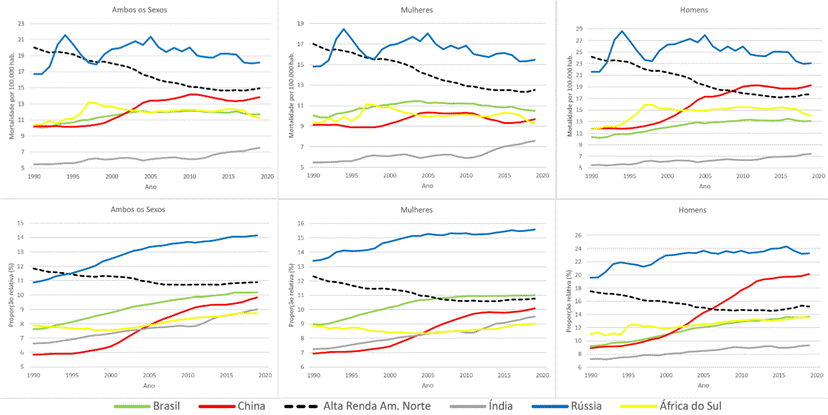
Figura 1. Taxas de mortalidade padronizadas por idade e proporção relativa de câncer colorretal em relação a todas as mortes por neoplasias, estratificado por sexo no Brasil, Rússia, Índia, China, África do Sul e nos países de alta renda da América do Norte de 1990 a 2019
A Figura 2 resume a variação percentual anual das taxas de mortalidade (net drift) e as diferenças etárias correspondentes (local drift). Entre 1990 e 2019, apenas a Rússia apresentou declínio global (-0,6%/ano), com queda mais acentuada nas mulheres (-1,0%/ano). Brasil e China exibiram os maiores aumentos médios (+0,7%/ano cada), seguidos pela Índia (+0,6%) e por uma oscilação não significativa na África do Sul.
Por sexo, o crescimento masculino foi expressivo na China (+1,8%/ano) e no Brasil (+1,0%/ano); a mortalidade feminina caiu na Rússia e na China, mas subiu no Brasil e na Índia.
No padrão etário (local drift), destacaram-se aumento feminino de 30-39 anos e masculino de 45-54 anos na África do Sul; queda de 45-54 anos em ambos os sexos na Rússia; e elevação persistente de 50-59 anos entre homens chineses. Tais padrões apontam coortes economicamente ativas como alvo prioritário nos países em ascensão e sugerem a eficácia das estratégias russas iniciadas nos anos 2000 (Figura 2).
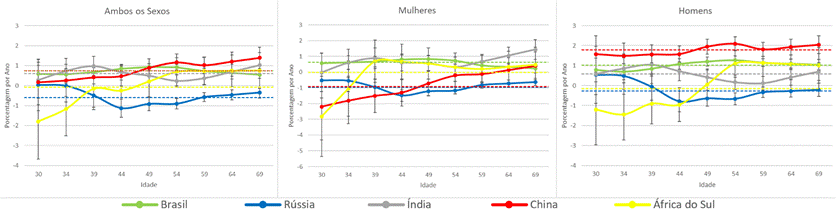
Figura 2. Local drift* com valores de net drift* para mortalidade por CCR estratificado por sexo no Brasil, Rússia, Índia, China e África do Sul, na população de 30 a 69 anos, de 1990 a 2019
Nota: *O net drift (linha pontilhada) representa a variação percentual anual geral, e os valores de local drift (linha contínua) representam a variação percentual anual em cada faixa etária. Valores abaixo de 0 indicaram reduções na mortalidade por CCR ao longo do período do estudo.
A análise IPC confirmou o forte gradiente etário do CCR: em todos os BRICS as taxas cresceram exponencialmente com a idade, culminando aos 65-69 anos. O contraste foi máximo na Rússia, onde esse grupo apresentou risco dez vezes maior que aos 40 anos, e mínimo na Índia (Figura 3).
Os efeitos de período diferiram. No Brasil o aumento foi rápido até o início dos anos 2000, depois estabilizou-se com leve queda feminina. A Rússia registrou pequeno incremento inicial e declínio contínuo desde 2000, mais forte nas mulheres. A Índia manteve estabilidade até meados dos anos 2000 e depois passou a crescer em ambos os sexos. Na China, as mulheres prolongaram o declínio iniciado em 1990, enquanto os homens subiram até 2009 e, então, estabilizaram. A África do Sul variou pouco, exibindo pico masculino nos anos 1990, atenuado após 2000.
Quanto às coortes, o risco aumentou entre homens do Brasil, China e Índia, sobretudo nas gerações pós-1960 chinesas, enquanto caiu quase linearmente nas mulheres russas e chinesas. A África do Sul mostrou padrão irregular, com picos nas coortes de 1930-40, 1950-60 e 1970-80. Assim, o crescimento recente no BRICS concentra-se em homens de coortes jovens, ao passo que a Rússia apresenta reduções sistêmicas que beneficiam todos os grupos, principalmente o feminino (Figura 3).
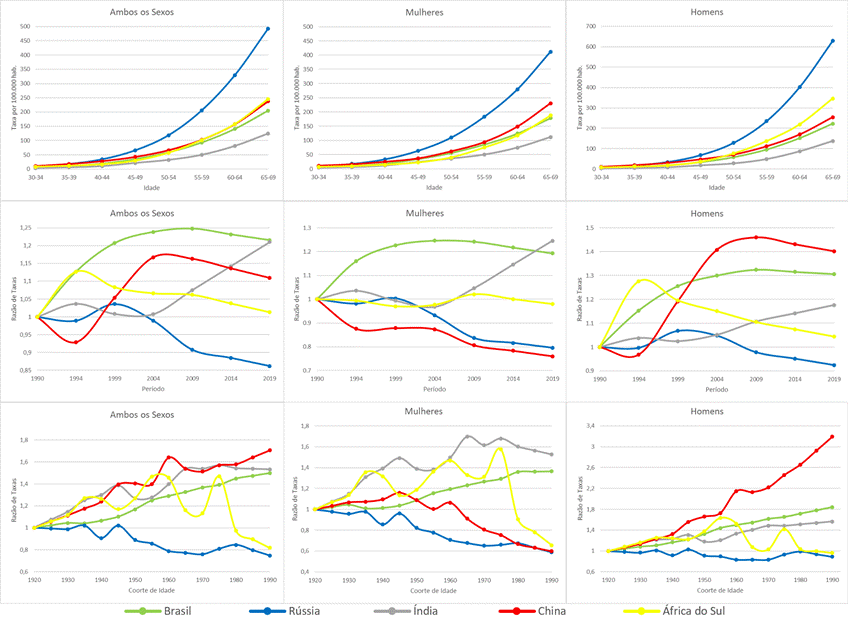
Figura 3. Estimativas dos efeitos de idade, período e de coorte de idade para mortalidade por câncer colorretal, estratificados por sexo, no Brasil, Rússia, Índia, China e África do Sul de 1990 a 2019
Entre 1990 e 2019, os países membros originais do BRICS apresentaram trajetórias de mortalidade por CCR heterogêneas, reflexo dos diferentes estágios de transição demográfica e epidemiológica e da eficácia variável dos seus sistemas de saúde. Nos países de alta renda, as taxas têm caído graças ao rastreamento populacional e a avanços terapêuticos, ao passo que nações de média e baixa rendas ainda exibem aumento6,7. No bloco, predominou o crescimento das mortes por CCR, mas em ritmos diversos, com sinais recentes de estabilização ou declínio onde políticas de controle foram reforçadas.
Brasil
No Brasil, as taxas de mortalidade por CCR cresceram de forma consistente a partir de 1990, mas há sinais de desaceleração na última década. O aumento foi mais intenso entre 1990 e meados dos anos 2000; depois ocorreu estabilização e, nos anos 2010, discreto declínio. Uma análise do GBD identificou inflexão em 2011, com variação anual de –0,05% até 201923. O resultado sugere avanços na detecção precoce e na terapêutica oncológica oferecida pelo Sistema Único de Saúde (SUS) e as primeiras iniciativas de rastreamento. O país é um dos poucos de renda média latino-americanos com ações populacionais, como o programa-piloto paulista que combina teste imunológico de sangue oculto nas fezes e colonoscopia para pessoas de 50-74 anos24. Embora a cobertura ainda seja incipiente, entre 2000 e 2017, o Brasil teve a maior expansão da atenção primária entre os BRICS25, favorecendo o diagnóstico mais precoce.
Paradoxalmente, as Regiões Sul e Sudeste, economicamente mais desenvolvidas, concentram as maiores taxas. Em 2020, estimou-se cerca de dez mortes por 100 mil homens e oito por 100 mil mulheres nessas áreas, superando Norte e Nordeste26. O gradiente reflete maior urbanização, envelhecimento e prevalência de fatores de risco (dieta ocidental, sedentarismo, sobrepeso e obesidade)26,27, além de melhor acesso a serviços diagnósticos, que aumenta a identificação de casos e óbitos. Nas Regiões menos favorecidas, barreiras de acesso podem gerar sub-registro, apesar do crescimento real do risco associado à transição nutricional.
As desigualdades socioeconômicas internas também se manifestam entre grupos individuais: o aumento da mortalidade tem sido mais pronunciado nos estratos de menor renda, que historicamente apresentavam risco baixo, mas hoje acumulam fatores de risco e dispõem de menor acesso ao rastreamento e ao tratamento. Para mitigar essas disparidades, o Ministério da Saúde lançou o Plano de Expansão da Radioterapia e o Plano de Ações Estratégicas para o Enfrentamento das Doenças Crônicas Não Transmissíveis, ambos com metas específicas para o CCR28,29. Contudo, avaliações recentes indicam que a meta de reduzir a mortalidade em 2% ao ano ainda não foi alcançada8, apontando para a necessidade de organizar programas de rastreamento, agilizar o tratamento e enfrentar os determinantes regionais e sociais da doença.
Rússia
A Rússia enfrenta carga crescente de CCR desde os anos 1990, impulsionada pelo envelhecimento populacional e mudanças comportamentais pós-soviéticas. O tumor já figura entre as principais causas de morte oncológica: segunda em mulheres (atrás do câncer de mama) e terceira em homens (após pulmão e estômago). Entre 1993 e 2019, a incidência padronizada subiu de 16,9 para 24,3/100 mil em mulheres e de 22,7 para 35,3/100 mil em homens, indicando acréscimo substancial na carga da doença28. Paralelamente, a razão de dependência de idosos aumentou de 18% em 2000 para 23,5% em 2020, ampliando o contingente vulnerável30.
Apesar das recomendações internacionais, o CCR não constava das prioridades nacionais de rastreamento nos anos 200031. Naquele período, cerca de 25% dos pacientes já apresentavam estádio IV ao diagnóstico e um terço morria no primeiro ano – sinais de detecção tardia e acesso limitado ao tratamento31.
Reformas iniciadas em 2011 incluíram o CCR nas consultas de rotina e, em 2013, colonoscopias passaram a ser cobertas pelo sistema público32. O Plano Nacional de Controle do Câncer33 definiu diretrizes clínicas, parâmetros assistenciais e orçamento para prevenção, diagnóstico e tratamento. Embora essas ações tenham contribuído para a queda recente observada nas taxas de mortalidade, os níveis permanecem altos. Estudos de 202234,35 ainda relatam barreiras no acesso à oncologia, ausência de programas organizados de rastreamento e alta proporção de casos avançados34. Por outro lado, relatos mais recentes destacam melhorias no atendimento especializado e redução do estadiamento tardio35.
Índia
Historicamente, a Índia registrava baixas taxas de CCR, mas a incidência e a mortalidade vêm subindo com a transição epidemiológica e nutricional da população36. Em 2022, o tumor já era o quarto mais frequente (64.863 novos casos) e causou aproximadamente 38.367 óbitos, evidenciando elevada letalidade; enquanto nos países de alta renda as taxas caem, várias Regiões indianas mostram tendência ascendente6. Centros urbanos e Estados economicamente mais avançados concentram maior incidência e mortalidade que zonas rurais, refletindo diferenças de estilo de vida e de acesso a cuidados37. Entre 2000-2019, a mortalidade nacional cresceu em média +0,02%/ano (ambos os sexos), com aumento mais evidente entre mulheres; mesmo modesta, essa variação implica grande número absoluto de vidas perdidas em razão do tamanho populacional38.
O avanço do CCR se relaciona com o envelhecimento demográfico, difusão de dietas ocidentais (menor vegetarianismo, mais carnes processadas, gorduras e açúcar) e aumento do sedentarismo e da obesidade, sobretudo na classe média urbana6. Em seu sistema de saúde, a Índia apresenta a menor cobertura de atenção primária e o menor gasto público em saúde do BRICS23,36, com um setor privado que domina a prestação de serviços em todas as faixas de renda, enquanto o sistema público permanece fragilizado39. Esse arranjo torna o tratamento oncológico financeiramente proibitivo para muitos: o custo semanal de radioterapia, com ou sem quimioterapia, pode equivaler a 60% da renda mensal média40,41.
Políticas lançadas na década de 2010, como o National Cancer Control Programme, priorizaram neoplasias mais incidentes (orais, cervicais, mamárias), deixando o CCR sem abordagem programática robusta42. Para conter o avanço projetado, autores como Shaji et al.37 recomendam campanhas de conscientização sobre sintomas intestinais, expansão do saneamento (pela associação com doenças inflamatórias intestinais) e inclusão de testes de rastreamento nas políticas públicas.
China
A China viu as mortes anuais por CCR mais que dobrarem entre 1990 e 201911. Nesse intervalo, a taxa de mortalidade padronizada subiu de 10,2 para 13,9 por 100 mil habitantes, um aumento de 36%43, apesar dos avanços terapêuticos. A incidência cresceu ainda mais: entre os homens, passou de 14,2 para 41,4 por 100 mil9. Esse salto acompanha a urbanização acelerada, a adoção de dietas com maior consumo de carne vermelha e alimentos processados, o sedentarismo e o aumento da expectativa de vida9,44.
Apesar do forte incremento nos casos, há evidências de melhora gradual nos desfechos graças ao aperfeiçoamento do sistema de saúde. Nas últimas duas décadas, o país investiu fortemente no sistema de saúde, expandindo centros oncológicos, formando especialistas e ampliando a cobertura dos seguros. Em 2021, liderava o investimento em atenção primária entre os BRICS38. Isso pode ter contribuído para moderar o crescimento da mortalidade em relação à incidência, ou seja, embora mais pessoas estejam desenvolvendo CCR, uma proporção um pouco maior delas está sobrevivendo mais tempo ou sendo curada em comparação com o passado. Estudos em grandes cidades já sugerem estabilização ou leve queda da mortalidade45.
No âmbito da prevenção, o principal avanço foi o Programa de Rastreamento de Câncer em Áreas Urbanas, iniciado em 2012, que combina teste imunológico fecal e questionário de risco46. Entretanto, esses tipos de programas permanecem limitados em alcance. Estimativas recentes sugerem que apenas cerca de 2,7% da população elegível (idades 40–74 anos) participaram de algum programa organizado de rastreamento de CCR em 202047. Até 2022, não existia um programa nacional abrangente que cobrisse todo o país48. Isso significa que a maioria dos diagnósticos continua ocorrendo de forma sintomática. A China também não conta com um sistema de saúde público universal, como aquele visto no Brasil. Apesar de o país ter obtido mais de 95% de cobertura da população, somando seguros de saúde públicos e privados, até os meados dos anos 2010, sua política de reembolso dificultava o acesso de famílias mais pobres aos serviços de saúde40. Além disso, os seguros de saúde na China são associados ao sistema de moradia chinês (hùkǒu), dificultando o acesso a serviços de saúde quando o usuário se encontra fora de seu local oficial de residência em um país onde cerca de um quinto da população consiste em trabalhadores migrantes49.
África do Sul
A África do Sul apresenta perfil singular de CCR, marcado por diferenças históricas entre grupos populacionais. A população branca, com dieta e estilo de vida ocidentais, sempre exibiu incidência e mortalidade elevadas, enquanto a população negra mantinha taxas muito inferiores. Essa disparidade, porém, vem diminuindo: entre 2002-2014, a mortalidade por CCR cresceu em média 1,3% ao ano, impulsionada sobretudo por homens negros (+4,2%/ano) e mulheres negras (+3,4%/ano), ao passo que grupos de maior renda mostraram tendência estável7.
As razões para o aumento da mortalidade por CCR na África do Sul são multifatoriais. Do ponto de vista demográfico, a população negra, majoritária no país, passou por melhorias socioeconômicas e de saúde pós-1990 que levaram a maior longevidade, permitindo que mais indivíduos atinjam idades em que o CCR se torna prevalente. Paralelamente, a urbanização e a globalização dos hábitos alimentares influenciaram mudanças de dieta também nessa população, com maior consumo de alimentos processados e de origem animal e redução na ingestão de fibras, além de aumento no sedentarismo. Esses fatores de risco, antes pouco comuns entre negros sul-africanos, estão associados ao crescimento da incidência de CCR, conforme observado em outras partes da África em transição50.
Na África do Sul, ainda persistem grandes desigualdades no acesso à saúde. Seu sistema é dual, com um setor privado bem estruturado, voltado à minoria de maior renda, e um setor público com recursos limitados. No privado, exames como colonoscopia de rastreamento e tratamento precoce são mais frequentes; enquanto na rede pública, diagnósticos costumam ocorrer tardiamente. Até 2020, não havia programa público de rastreamento populacional. As políticas nacionais incluem promoção de dieta saudável e atividade física, mas ainda sem diretrizes específicas para CCR51. Iniciativas pontuais, como unidades móveis de colonoscopia, permanecem experimentais, e a maioria dos casos segue detectada tardiamente, contribuindo para alta letalidade52.
É importante salientar algumas das limitações impostas a esta análise, tais como: a) este estudo utiliza estimativas do GBD, sujeitas a variações na qualidade dos registros de óbitos entre os BRICS e a possíveis vieses residuais, além de empregar um modelo IPC que, por requerer restrições para resolver colinearidade, fornece efeitos essencialmente ecológicos sensíveis à parametrização; b) o trabalho com dados nacionais e intervalos quinquenais também oculta disparidades regionais e pode suavizar variações sutis; e c) a falta de informações individuais de incidência e sobrevida impede distinguir mudanças na ocorrência da doença de avanços terapêuticos. Pesquisas futuras devem reunir informações de mortalidade, incidência e sobrevida em escala regional e individual para refinar a compreensão das tendências do CCR nos diferentes contextos dos BRICS.
CONCLUSÃO
Entre 1990 e 2019, as taxas padronizadas de mortalidade por CCR caíram nos países de alta renda da América do Norte, mas cresceram cerca de um quarto no conjunto dos países membros originais do BRICS, com marcada heterogeneidade interna: aumento expressivo na China e na Índia, estabilização recente no Brasil, declínio sustentado na Rússia e variação discreta na África do Sul. A análise IPC demonstrou que o acréscimo de mortalidade se concentra sobretudo em homens pertencentes a coortes pós-1960 e em faixas etárias economicamente ativas, ao passo que a Rússia exemplifica o potencial de políticas de controle para reverter a tendência.
Os achados indicam que iniciativas de rastreamento organizado, ampliação do acesso ao diagnóstico precoce e redução de fatores de risco comportamentais são prioritárias nos países em que a mortalidade continua a subir, especialmente para populações masculinas e coortes jovens. No caso do Brasil, o fortalecimento de programas já em curso e a expansão equitativa da cobertura são estratégias plausíveis; na China, o desafio é escalar pilotos de rastreamento; na Índia e na África do Sul, estabelecer políticas nacionais de detecção precoce e superar barreiras de custo e acesso; e, na Rússia, consolidar os ganhos obtidos. Ao fornecer uma comparação padronizada entre grandes economias emergentes, este estudo busca contribuir com evidências que podem orientar o planejamento oncológico e a alocação de recursos nos BRICS, reforçando a necessidade de abordagens adaptadas às trajetórias demográficas, epidemiológicas e sistêmicas de cada país.
AGRADECIMENTOS
Aos professores Eduardo Rodrigues Gomes (UFF), Washington Leite Junger (Uerj) e Gulnar Azevedo e Silva (Uerj) pelas contribuições na revisão deste artigo.
CONTRIBUIÇÕES
Marcus Verly-Miguel contribuiu na concepção e no planejamento do estudo; na obtenção, análise e interpretação dos dados; e na redação. Caroline Madalena Ribeiro contribuiu na concepção e no planejamento do estudo; e na revisão crítica. Ambos os autores aprovaram a versão final a ser publicada.
DECLARAÇÃO DE CONFLITOS DE INTERESSE
Nada a declarar.
DECLARAÇÃO DE DISPONIBILIDADE DE DADOS
Os conjuntos de dados gerados e analisados durante o estudo atual estão disponíveis nas URL "https://www.healthdata.org/data-visualization/gbd-results" e " https://population.un.org/wpp/downloads?folder=Standard%20Projections&group=Population".
FONTES DE FINANCIAMENTO
Marcus Verly-Miguel foi bolsista Proex durante a produção deste artigo.
REFERÊNCIAS
1. Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2024;74(3):229-63. doi: https://doi.org/10.3322/caac.21834
2. Arnold M, Sierra MS, Laversanne M, et al. Global patterns and trends in colorectal cancer incidence and mortality. Gut. 2017;66(4):683-91. doi: https://doi.org/10.1136/gutjnl-2015-310912
3. Jin X, Dong D, Xu Z, et al. The global burden of colorectal cancer attributable to high body-mass index in 204 countries and territories: findings from 1990 to 2021 and predictions to 2035. Front Nutr. 2024;11:1473851. doi: https://doi.org/10.3389/fnut.2024.1473851
4. Jakovljevic M, Lamnisos D, Westerman R, et al. Future health spending forecast in leading emerging BRICS markets in 2030: health policy implications. Health Res Policy Syst. 2022;20(1):23. doi: https://doi.org/10.1186/s12961-022-00822-5
5. Pearce A, Sharp L, Hanly P, et al. Productivity losses due to premature mortality from cancer in Brazil, Russia, India, China, and South Africa (BRICS): a population-based comparison. Cancer Epidemiol. 2018;53:27-34. doi: https://doi.org/10.1016/j.canep.2017.12.013
6. Shivshankar S, Patil PS, Deodhar K, et al. Epidemiology of colorectal cancer: a review with special emphasis on India. Indian J Gastroenterol. 2025;44:142-53. doi: https://doi.org/10.1007/s12664-024-01726-8
7. Motsuku L, Chen WC, Muchengeti MM, et al. Colorectal cancer incidence and mortality trends by sex and population group in South Africa: 2002-2014. BMC Cancer. 2021;21(1):129. doi: https://doi.org/10.1186/s12885-021-07853-1
8. Tofani AA, Verly-Miguel MVB, Marques MC, et al. Mortalidade por Câncer de Cólon e Reto no Brasil e suas Regiões entre 2006 e 2020. Rev Bras Cancerol. 2024;70(1):e-074404. doi: https://doi.org/10.32635/2176-9745.RBC.2024v70n1.4404
9. Li Q, Wu H, Cao M, et al. Colorectal cancer burden, trends and risk factors in China: a review and comparison with the United States. Chin J Cancer Res. 2022;34(5):483-95. doi: https://doi.org/10.21147/j.issn.1000-9604.2022.05.08
10. Nath A, Taneja R, Thadi YS, et al. A comparative study of incidence, mortality and disability adjusted life years (DALYs) for leading cancers in BRICS countries. ecancermedicalscience [Internet]. 2024 [acesso 2025 jun 6];18. Disponível em: https://ecancer.org/en/journal/article/1773-a-comparative-study-of-incidence-mortality-and-disability-adjusted-life-years-dalys-for-leading-cancers-in-brics-countries
11. Sharma R, Abbasi-Kangevari M, Abd-Rabu R, et al. Global, regional, and national burden of colorectal cancer and its risk factors, 1990-2019: a systematic analysis for the Global Burden of Disease Study 2019. Lancet Gastroenterol Hepatol. 2022;7(7):627-47. doi: https://doi.org/10.1016/s2468-1253(22)00044-9
12. Chen Y, Yang C, Li N, et al. Effects of population aging on the mortality burden of related cancers in urban and rural areas of China, 2004-2017: a population-based study. Cancer Biol Med. 2022;19(5):696-706. https://doi.org/10.20892/j.issn.2095-3941.2021.0538
13. Wang H, Abbas KM, Abbasifard M, et al. Global age-sex-specific fertility, mortality, healthy life expectancy (HALE), and population estimates in 204 countries and territories, 1950-2019: a comprehensive demographic analysis for the Global Burden of Disease Study 2019. The Lancet. 2020;396(10258):1160-203.
14. Liu D, Liu H, Wu Y, et al. Time trends in stomach cancer mortality across the BRICS: an age-period-cohort analysis for the GBD 2021. Front Public Health. 2025;13:1506925.
15. GBD Results [Internet]. Seattle: IHME; 2025 [acesso 2025 jun 25]. Disponível em: https://www.healthdata.org/data-tools-practices/interactive-visuals/gbd-results
16. Xi Y, Xu P. Global colorectal cancer burden in 2020 and projections to 2040. Transl Oncol. 2021;14(10):101174.
17. Department of Economic and Social Affairs Population Division [Internet]. Washington, DC: ONU; [sem data]. [acesso 2025 jun 26]. Disponívl em: https://population.un.org/wpp/downloads?folder=Standard%20Projections&group=Population
18. Holford TR. Understanding the effects of age, period, and cohort on incidence and mortality rates. Annu Rev Public Health. 1991;12(1):425-57.
19. Zou Z, Liu G, Hay SI, et al. Time trends in tuberculosis mortality across the BRICS: an age-period-cohort analysis for the GBD 2019. eClinicalMedicine. 2022;53:101646. doi: https://doi.org/10.1016/j.eclinm.2022.101646
20. Rosenberg PS, Check DP, Anderson WF. A web tool for age–period–cohort analysis of cancer incidence and mortality rates. Cancer Epidemiol Biomarkers Prev. 2014;23(11):2296-302. doi: https://doi.org/10.1158/1055-9965.epi-14-0300
21. Banner for NCI Division of Cancer Epidemiology and Genetics Biostatistics Branch [Internet]. Washington, DC: NIH; [sem data]. [acesso 2025 jun 26]. Disponívl em: https://analysistools.cancer.gov/apc/
22. Conselho Nacional de Saúde (BR). Resolução n° 510, de 7 de abril de 2016. Dispõe sobre as normas aplicáveis a pesquisas em Ciências Humanas e Sociais cujos procedimentos metodológicos envolvam a utilização de dados diretamente obtidos com os participantes ou de informações identificáveis ou que possam acarretar riscos maiores do que os existentes na vida cotidiana, na forma definida nesta Resolução [Internet]. Diário Oficial da União, Brasília, DF. 2016 maio 24 [acesso 2025 abr 7]; Seção 1:44. Disponível em: http://bvsms.saude.gov.br/bvs/saudelegis/cns/2016/res0510_07_04_2016.html
23. Muzi CD, Banegas MP, Guimarães RM. Colorectal cancer disparities in Latin America: mortality trends 1990-2019 and a paradox association with human development. PLoS One. 2023;18(8):e0289675. doi: https://doi.org/10.1371/journal.pone.0289675
24. Filogonio V, Maia YR, Maia LH. The challenge of colorectal cancer (CRC) screening in low and middle-income countries (LMIC): the brazilian ten year long experience. JCO Glob Oncol. 2023;9(Sup1):129.
25. World Health Organization. Global Health Expenditure Database [Internet]. Genebra: WHO; 2025 [acesso 2025 jun 9]. Disponível em: https://apps.who.int/nha/database/PHC_Country_profile/Index/en
26. Monteiro dos Santos JE, Campos Araújo M, Marcelo Furtado Passos Da Silva C. Overweight is the main behavioral risk factor associated with colorectal cancer mortality in the Brazilian population: an ecological analysis. Sci Rep. 2024;14(1):28178. doi: https://doi.org/10.1038/s41598-024-79921-y
27. Silva GAE, Jardim BC, Ferreira VDM, et al. Mortalidade por câncer nas capitais e no interior do Brasil: uma análise de quatro décadas. Rev Saúde Pública. 2020;54:126. doi: https://doi.org/10.11606/s1518-8787.2020054002255
28. Ministério da Saúde (BR) [Internet]. Brasília, DF: MS; 2000. Plano de Expansão da Radioterapia no SUS, 2017 [acesso 2025 jun 9]. Disponível em: https://www.gov.br/saude/pt-br/acesso-a-informacao/acoes-e-programas/per-sus/plano-de-expansao-da-radioterapia-no-sus
29. Malta DC, Morais Neto OLD, Silva Junior JBD. Apresentação do plano de ações estratégicas para o enfrentamento das doenças crônicas não transmissíveis no Brasil, 2011 a 2022. Epidemiol Serv Saúde. 2011;20(4):425-38. doi: https://doi.org/10.5123/S1679-49742011000400002
30. Barchuk A, Raskina Y, Tursun-Zade R, et al. Cancer on the global stage: incidence and cancer-related mortality in the Russian federation [Internet]. 2022 [acesso 2025 jun 9]. Disponível em : https://ascopost.com/issues/february-10-2022/cancer-on-the-global-stage-incidence-and-cancer-related-mortality-in-the-russian-federation/
31. Avksentyeva M. Colorectal cancer in Russia. Eur J Health Econ. 2010;10(S1):91-8.
32. Rekhter N, Ermasova N. Culture of prevention and early disease detection of cancer in Russia. Soc Sci Med. 2021;277:113905. doi: https://doi.org/10.1016/j.socscimed.2021.113905
33. Petrovsky A, Tjulandin S, Tryakin A, et al. Creation and development of the National Cancer Control Plan in Russia. J Clin Oncol. 2019;37(supl15):10524.
34. Shishkin S, Sheiman I, Vlassov V, et al. Structural changes in the Russian health care system: do they match European trends? Health Econ Rev. 2022;12(1):29.
35. Gordienko VP, Ilyushenok AS. Cancer incidence and mortality and state of cancer care for colorectal cancer patients in the Russian Far East. Sib J Oncol. 2022;21(5):5-16.
36. Mohandas KM. Colorectal cancer in India: controversies, enigmas and primary prevention. Indian J Gastroenterol. 2011;30(1):3-6.
37. Shaji A, Keechilat P, Dk V, et al. Analysis of the mortality trends of 23 major cancers in the indian population between 2000 and 2019: a joinpoint regression analysis. JCO Glob Oncol. 2023;(9):e2200405. doi: https://doi.org/10.1200/go.22.00405
38. World Health Organization [Internet]. Geneva: [sem data]. The global health observatory-UHC service coverage index (SDG 3.8.1), 2023 [acesso 2025 jun 9]. Disponível em: https://www.who.int/data/gho/data/indicators/indicator-details/GHO/uhc-index-of-service-coverage
39. Mackintosh M, Channon A, Karan A, et al. What is the private sector? Understanding private provision in the health systems of low-income and middle-income countries. The Lancet. 2016;388(10044):596-605.
40. Goss PE, Strasser-Weippl K, Lee-Bychkovsky BL, et al. Challenges to effective cancer control in China, India, and Russia. Lancet Oncol. 2014;15(5):489-538.
41. Mohanti BK, Mukhopadhyay A, Das S, et al. Estimating the economic burden of cancer at a tertiary public hospital: a study at the all India Institute of Medical Sciences [Internet]. [sem local]: Indian Statistical Institute; 2011 [acesso 2025 jun 9]. Disponível em: https://www.isid.ac.in/~abhiroop/res_papers/WORKING_PAPERS_files/cancer.pdf
42. Tewari M. Cancer care in India. Indian J Endocr Surg Res. 2022;17(1):1-3.
43. Zhai G, Wang Y. Disease burden of colorectal cancer in China from 1990 to 2019: age- and sex-specific time trends and 10-year forecast. Oncol Res Treat. 2024;47(3):76-87.
44. Yuan M, Seale Jr JL, Wahl T, et al. The changing dietary patterns and health issues in China. China Agric Econ Rev. 2019;11(1):143-59.
45. Ong SS, Xu L, Deng X, et al. Trends, global comparisons, and projections of early onset colorectal cancer burden in China based on GBD study 2021. Sci Rep. 2025;15(1):2969.
46. Dong X, Du L, Luo Z, et al. Combining fecal immunochemical testing and questionnaire-based risk assessment in selecting participants for colonoscopy screening in the Chinese National Colorectal Cancer Screening Programs: a population-based cohort study. Plos Med. 2024;21(2):e1004340. doi: https://doi.org/10.1371/journal.pmed.1004340
47. Li Y, Wang X, Wu Y, et al. Access to colorectal cancer screening in populations in China, 2020: a coverage‐focused synthesis analysis. Int J Cancer. 2024 Aug;155(3):558-68.
48. Chen H, Lu B, Dai M, Colorectal cancer screening in China: status, challenges, and prospects - China, 2022. China CDC Wkly. 2022;4(15):322-8. doi: https://doi.org/10.46234/ccdcw2022.077
49. Chen S, Chen Y, Feng Z, et al. Barriers of effective health insurance coverage for rural-to-urban migrant workers in China: a systematic review and policy gap analysis. BMC Public Health. 2020;20(1):408. doi: https://doi.org/10.1186/s12889-020-8448-8
50. Awedew AF, Asefa Z, Belay WB. Burden and trend of colorectal cancer in 54 countries of Africa 2010-2019: a systematic examination for global burden of disease. BMC Gastroenterol. 2022;22(1):204. doi: https://doi.org/10.1186/s12876-022-02275-0
51. Magwaza S, Van Hal G, Hoque M. National Cancer Control Plans: comparative analysis between South Africa and Brazil focusing on colorectal cancer control. J Gastrointest Dig Syst. 2020;10(6):1-8.
52. Laiyemo AO, Brawley O, Irabor D, et al. Toward colorectal cancer control in Africa. Int J Cancer. 2016;138(4):1033-4.
Recebido em 31/7/2025
Aprovado em 17/9/2025
Editora associada: Jeane Tomazelli. Orcid iD: https://orcid.org/0000-0002-2472-3444
Editora-científica: Anke Bergmann. Orcid iD: https://orcid.org/0000-0002-1972-8777
Este é um artigo publicado em acesso aberto (Open Access) sob a licença Creative Commons Attribution, que permite uso, distribuição e reprodução em qualquer meio, sem restrições, desde que o trabalho original seja corretamente citado.